Introducción
El trasplante de hígado (TH) se considera en la actualidad el tratamiento de elección de la insuficiencia hepática crónica, la falla hepática aguda con indicadores de mal pronóstico, tumores hepáticos primarios adecuadamente seleccionados y en algunas enfermedades por errores en el metabolismo 1. Han existido grandes avances desde 1963 cuando el Dr. Thomas Starzl realizó el primer TH en humanos 2, inicialmente con resultados decepcionantes pero que en la actualidad han mejorado por el perfeccionamiento de las técnicas quirúrgicas, mejores cuidados perioperatorios, la utilización de nuevos y más efectivos medicamentos inmunosupresores y la adecuada selección de los pacientes. En un reciente estudio de Thuluvath sobre los resultados de centros americanos a largo plazo (información OPTN/SRTR), se encontró que la sobrevida de pacientes a 1, 5 y 10 años es de 88.4, 73.8 y 60% respectivamente 3. A pesar de estos resultados favorables, los pacientes sometidos a TH pueden tener complicaciones graves que pueden llevar incluso a la muerte, como son las infecciones, las complicaciones vasculares y las complicaciones biliares 4. En Colombia, desde finales de los 90s hasta el 2011 se han realizado más de 1700 trasplantes de hígado 5, sin que hasta el momento exista una información confiable de los resultados de sobrevida ni de las complicaciones que se presentan en estos pacientes, por lo cual se reporta la experiencia del grupo de trasplante hepático del Hospital Pablo Tobón Uribe en Medellín - Colombia.
Materiales y Métodos
Desde febrero de 2004 hasta diciembre de 2010 se realizaron 305 trasplantes ortotópicos de hígado en el Hospital Pablo Tobón Uribe de Medellín, 272 adultos y 33 niños, en todos ellos con donante cadavérico. En 241 pacientes adultos se efectuó trasplante hepático por primera vez. Este es un estudio descriptivo retrospectivo que incluyó todos los pacientes con trasplante hepático en adultos y fueron excluidos los pacientes pediátricos, retrasplantes y trasplantes multiviscerales. Nuestro equipo multidisciplinario de trasplante hepático de adultos está constituido por 3 cirujanos de trasplante, 4 hepatólogos, 4 anestesiólogos, 1 trabajadora social, 1 psicóloga y un coordinador de enfermería. Los datos demográficos, así como de morbilidad y de mortalidad fueron obtenidos por revisión retrospectiva de las historias clínicas y de la base de datos de trasplante hepático, autorizado por el comité de ética del hospital. En todos los pacientes se estratificó la severidad de la enfermedad hepática con el puntaje Child-Turcotte-Pugh (Child) y el puntaje MELD. Todos los pacientes con carcinoma hepatocelular (CHC) debían cumplir los criterios de Milán para ser sometidos al trasplante. Los individuos con falla hepática aguda se trasplantaron cuando cumplieron los criterios de mal pronóstico del hospital King´s Collage. La inmunosupresión convencional consistió en Ciclosporina o Tacrolimus, Azatioprina o Micofenolato mofetil y esteroides, suspendiendo estos últimos entre los 3 a 6 meses después del procedimiento. Se buscó retirar la Azatioprina o el Micofenolato mofetil después del primer año, excepto en los casos de enfermedad hepática auto inmune. Los individuos con IgG para Citomegalovirus (CMV) donante positivo/receptor negativo se manejaron con profilaxis de ganciclovir/valganciclovir durante los primeros tres meses. Los pacientes con infección crónica por hepatitis B continuaron con el antiviral oral y se adicionó inmunoglobulina intramuscular contra hepatitis B de manera indefinida. En caso de rechazo agudo moderado a severo confirmado por biopsia se realizó tratamiento con bolos de metilprednisolona. Algunos pacientes con disfunción renal que no eran candidatos a trasplante combinado de hígado y riñón, Child B o C y con ascitis recibieron Basiliximab para permitir introducir más tardíamente el inhibidor de la calcineurina. La técnica quirúrgica de la vena cava fue Piggy-back, sin necesidad de bypass veno-venoso en ningún paciente. La anastomosis biliar convencional fue colédoco-coledocostomía, sin uso de tubo en T y con hepático-yeyunostomía a criterio del cirujano de trasplante. Todos los pacientes se trasladaron en el post operatorio a la unidad de cuidado intensivo (UCI), implementándose un protocolo de extubación temprana.
El análisis estadístico partió de las descripciones de las diferentes variables socio demográficas y clínicas de los pacientes en estudio, entre las que se incluyeron condiciones pre trasplante, etiología de la enfermedad hepática, severidad del cuadro clasificada por Child y MELD, variables intraoperatorias y variables postoperatorias como complicaciones, días en UCI, estancia hospitalaria, sobrevida del injerto y de pacientes. Inicialmente se verificó el tipo de distribución de las variables y se realizó un análisis bivariado usando prueba de X2 para variables categóricas y la prueba no paramétrica U de Mann-Whitney para comparar rangos entre grupos independientes. Se realizó un análisis de supervivencia utilizando la curva de Kaplan Meier para los desenlaces de pérdida de injerto y muerte del paciente, a 1 y 5 años, en ambos casos.
Resultados
Datos generales
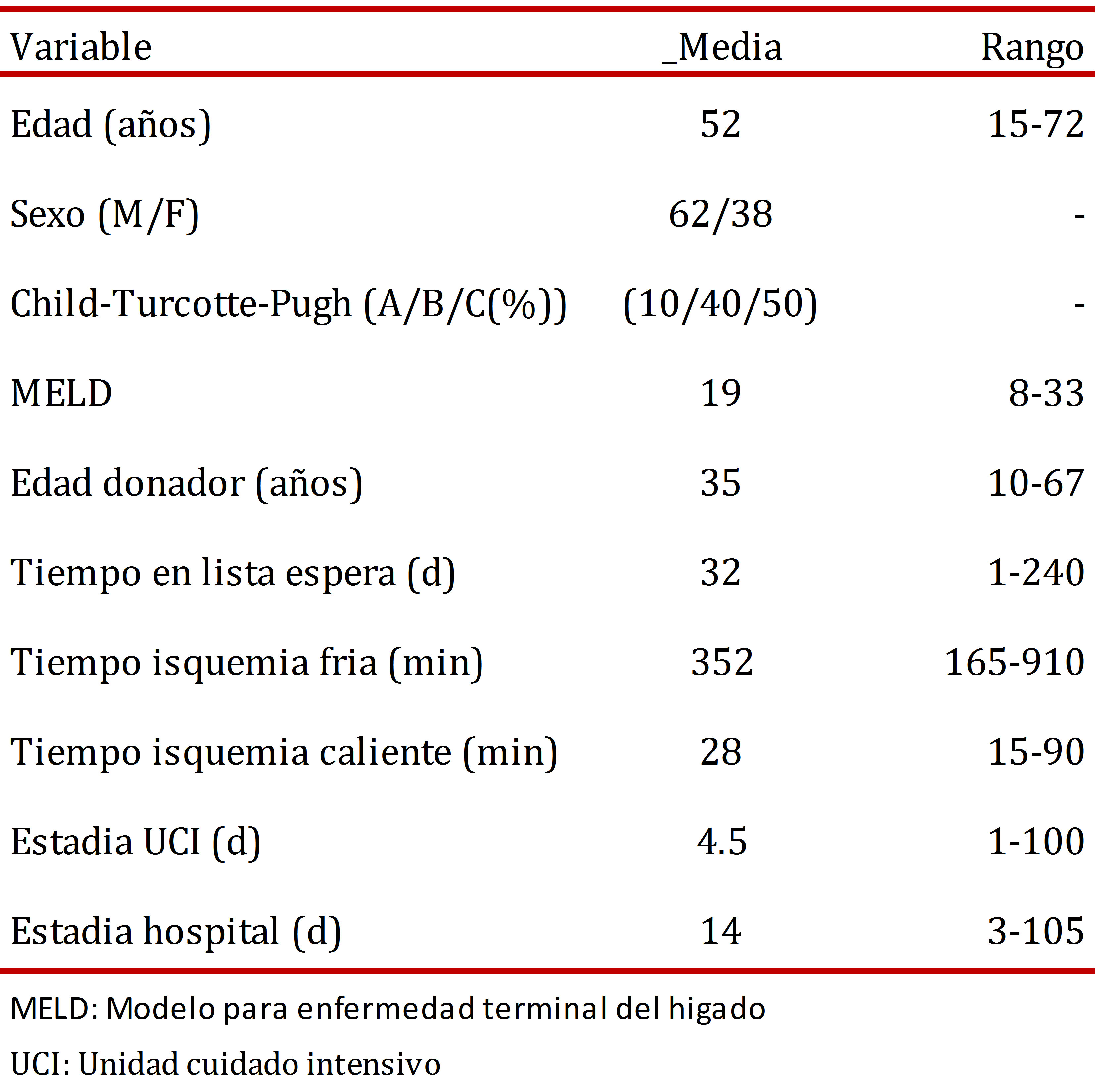
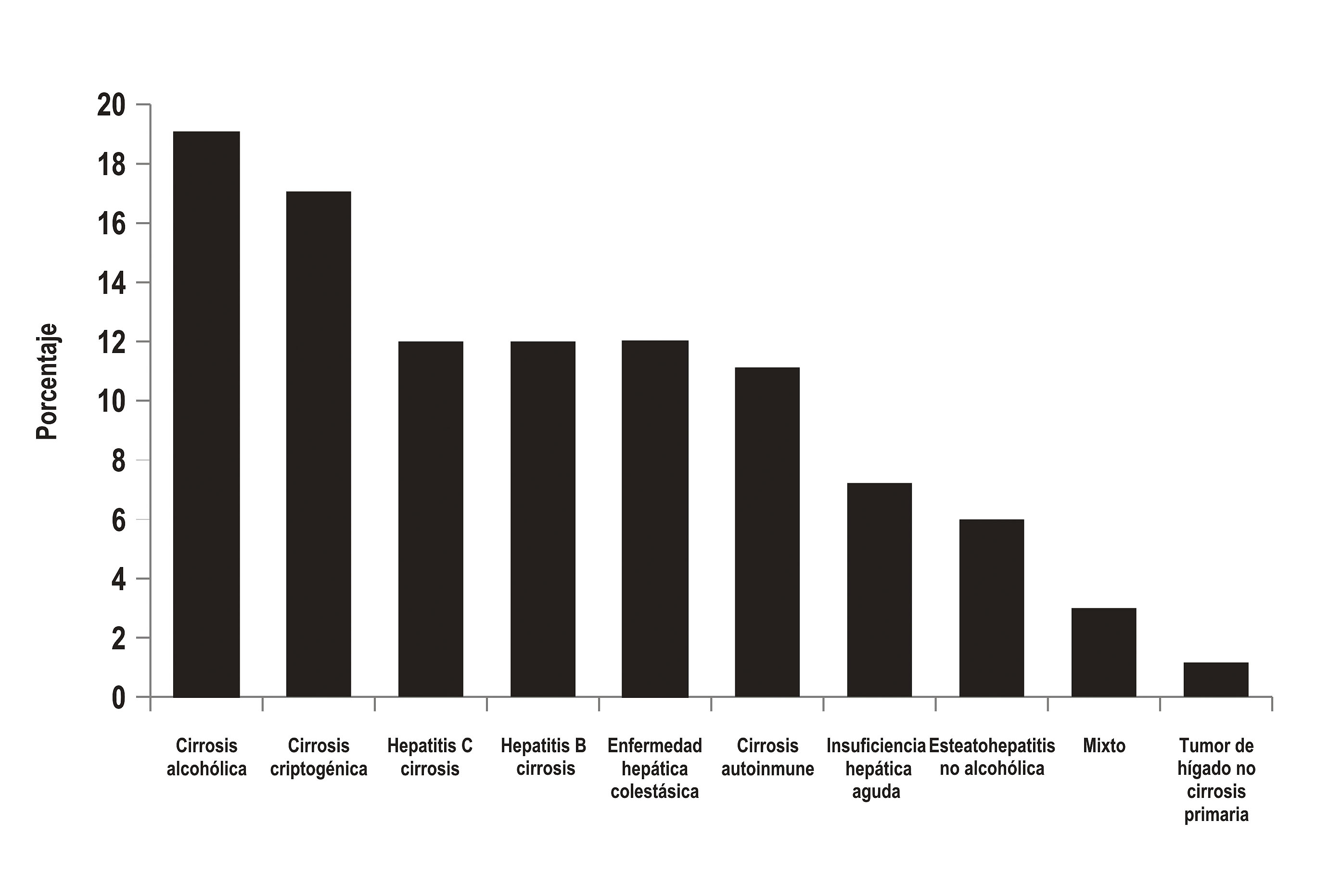
La edad promedio de los receptores fue de 52 años (rango 15-72 años) y el 62% fueron de sexo masculino. El 50% de los pacientes eran Child C y el score MELD promedio fue de 19. La etiología de la enfermedad hepática se describe en la Figura 1. El 80% de los pacientes que se trasplantaron eran cirróticos y la principal causa fue la enfermedad hepática por alcohol. En el 15% de los casos la indicación del trasplante hepático fue el CHC y en el 7% fue la falla hepática aguda. En los casos denominados etiología mixta, se incluyen pacientes con hemocromatosis, enfermedad de Wilson, poliquistosis hepática, amiloidosis y síndrome de Budd Chiari. Además, se trasplantaron dos pacientes con tumor hepático primario sin cirrosis, uno con CHC fibrolamelar y otro con hemangioendotelioma epiteliode. Las características del donante y los tiempos quirúrgicos y de estancia hospitalaria se puede observar en la Tabla 1. La edad promedio de los donantes fue de 35 años, en el 60% de los casos la causa de muerte fue trauma craneoencefálico y en el 30% accidente cerebrovascular.
Figura 1.
Etiología de la enfermedad hepática en pacientes de trasplante hepático, Hospital Pablo Tobón Uribe, Medellín - Colombia, n: 241 pacientes.
Supervivencia
La supervivencia de pacientes a un año fue del 82% y a 5 años del 72% (Fig. 2). La supervivencia del injerto hepático fue 78% al primer año y 68% a los 5 años. La principal causa de muerte fue la sepsis, con otras causas descritas en la Tabla 2. El 40% de las muertes fueron tempranas, siendo su origen el sangrado masivo, la sepsis y la disfunción primaria del injerto. Las muertes por sangrado masivo ocurrieron durante los primeros dos años del inicio del programa de trasplante hepático, sin que en los últimos años se presentó muerte por esta causa. En las causas tardías de muerte se encontró la enfermedad cardiocerebrovascular y la falla renal.
Figura 2.
Supervivencia de pacientes de trasplante hepático, Hospital Pablo Tobón Uribe, Medellín - Colombia, n: 241 pacientes.

Complicaciones perioperatorias
Se presentó sangrado postoperatorio en el 22% de los pacientes, con necesidad de reintervención en el 20%. Síndrome de reperfusión se confirmó en el 2% de los pacientes, siendo la causa de muerte en un individuo. Disfunción primaria del injerto hepático se documentó en 11 pacientes (4.5%).
Complicaciones vasculares
Las complicaciones en la arteria hepática se presentaron en 13 pacientes (5%), siendo la trombosis temprana (primeros 30 días) la principal complicación (3.7%), en 5 pacientes con falla orgánica múltiple que llevo a la muerte. La estenosis de la arteria hepática se presentó en 4 pacientes y fue tardía en todos ellos, requiriendo manejo endovascular percutáneo. Las complicaciones en la vena porta se documentaron en 7 pacientes (3%), cinco de ellos con trombosis portal temprana (primeros 30 días). Un paciente se presentó con estenosis portal hemodinámicamente significativa, fue tardía y continúa con seguimiento sin evidencia disfunción del injerto hepático. Se encontraron complicaciones en las venas hepáticas o en el tracto de salida venoso en el 3% de los pacientes, ocurriendo más frecuentemente la estenosis que la trombosis, siendo uno de ellos reintervenido por lo temprano de la estenosis y los otros fueron tratados por vía endovascular con éxito del tratamiento.
Complicaciones biliares
Las complicaciones biliares se presentaron en 35 pacientes (14.5%). El 10% de las lesiones fueron estenosis anastomóticas de la vía biliar y en el 60% de los casos fueron tempranas (primeros 30 días). Estos pacientes se trataron por vía endoscopica con dilatación e implantación de prótesis biliares con éxito en más del 80% de los casos y solo algunos pacientes necesitaron reconstrucción quirúrgica. Las estenosis no anastomóticas de la vía biliar se documentaron en el 2% y todas fueron tardías. Las fugas biliares se encontraron en el 3% de los pacientes, presentándose casi en su totalidad concomitantemente con lesiones de estenosis. El 50% de los casos de complicaciones biliares se asociaron a procesos infecciosos originados en la vía biliar y en la cavidad abdominal.
Complicaciones infecciosas
El 41% de los pacientes presentaron alguna infección durante su evolución y en el 80% de los casos fueron tempranas (primeros 30 días). Infecciones bacterianas se documentaron en 84 pacientes (38%), originándose en abdomen en el 50% de los casos, donde se incluye la infección de la herida quirúrgica, colangitis y peritonitis. Otros focos en orden de frecuencia fueron el pulmón, el tracto urinario, las bacteriemias primarias y las infecciones de tejidos blandos. En cuanto a las infecciones virales, se documentó infección por Citomegalovirus (CMV) en el 10% de los pacientes y en el 80% de estos la presentación fue después del segundo mes. Se encontró infección por herpes Zoster en el 4% y herpes simple en 3%, siendo tardías en todas excepto en un caso. Infecciones micóticas invasivas se presentaron en 6 pacientes (2.5%). El principal germen fue Cándida no albicans, con origen en el tracto urinario en el 50%. Se diagnosticó en dos pacientes infección por Aspergillus. Uno de ellos con enfermedad pulmonar con diagnóstico precoz y tratamiento oportuno con resultado favorable, pero en el otro caso una enfermedad diseminada con endocarditis infecciosa y un diagnóstico tardío, con muerte del paciente a pesar del manejo quirúrgico y el tratamiento con voriconazol mas equinocandina. En dos pacientes se documentó tuberculosis (0.8%), ambos casos tardíos, uno de ellos en ganglios linfáticos y el otro con meningitis tuberculosa, con diagnóstico en las primeras semanas de aparición de los síntomas, tratamiento oportuno y exitoso sin causar la muerte en ningún individuo.
Otras complicaciones
Se encontró rechazo agudo probado por biopsia en 73 pacientes (30%). El 80% de estos rechazos agudos ocurrieron en los primeros tres meses, catalogados como leves a moderados por biopsia y por lo tanto no tuvieron mayor impacto en la sobrevida de los pacientes ni de los injertos. En cuanto al rechazo crónico, se presentó en 7 pacientes (3%), en el 85% de ellos precedido de rechazo agudo y en el 30% con pérdida del injerto a pesar del cambio de la inmunosupresión. Retrasplante hepático se realizó en el 6.6% de los pacientes, siendo las principales causas la colangiopatía isquémica, el rechazo crónico y la trombosis de la arteria hepática. En el 25% de los pacientes se desarrolló insuficiencia renal, en menos del 10% con necesidad de terapia de remplazo renal. Se encontró hipertensión arterial en el 27%, dislipidemia en 27%, diabetes mellitus en 8% y obesidad en 7%. Infección recurrente por Hepatitis C se presentó en todos los pacientes que se trasplantaron con carga viral positiva, aunque hepatitis crónica clínicamente significativa se presentó en el 30% de los pacientes, algunos recibieron tratamiento antiviral, un paciente necesitó retrasplante hepático y otros 2 pacientes murieron por la recurrencia de la enfermedad. En cuanto a la aparición de neoplasias de novo, se documentaron en 8 pacientes (3%), excluyendo las lesiones malignas de piel. De los pacientes con hepatocarcinoma se presentó recurrencia en el 8%, sin embargo solo uno de ellos presentó recurrencia severa con metástasis y muerte debido a la neoplasia.
Con respecto a la calidad de vida de los pacientes que fueron llevados a trasplante hepático no existió una evaluación formal, sin embargo nosotros documentamos que pacientes sin complicaciones serias retornaron rápidamente (después de tres meses) a sus actividades de la vida diaria, llevando una vida familiar normal incluyendo la posibilidad de ser padres y retornar al trabajo.
Discusión
El trasplante hepático ha sufrido múltiples modificaciones en los últimos años para generar los resultados actuales y desde hace 3 décadas es aceptada como una opción terapéutica de pacientes con enfermedad hepática avanzada 5. A pesar de que existen varios reportes de los resultados en diferentes centros en el mundo con más de 1,000 pacientes y más de 10 años de seguimiento, este es uno de los pocos documentos donde se reporta la experiencia en trasplante hepático de un centro en Latinoamérica.
En esta serie la supervivencia a 5 años de pacientes es del 72% y de los injertos hepáticos es del 68%, la cuales son comparables a las reportadas por registros oficiales en Estados Unidos y en Europa 3-6 , lo cual es relevante teniendo en cuenta la menor experiencia en nuestro país y las limitaciones económicas para este tipo de procedimientos.
Con respecto a otros reportes en la región, Buckel et al 7 y Castro et al 8 informan tasas de supervivencia similares desde Chile y Brasil, siendo este último país el séptimo en el mundo con número de trasplantes hepáticos 9. En los últimos años varios centros han documentado supervivencia de los pacientes al año superior al 90%, por lo cual nuestro propósito es lograr estos excelentes resultados.
En este estudio, la mortalidad en el primer año fue elevada, siendo las principales causas la sepsis con falla orgánica múltiple y el sangrado masivo, mejorando en los últimos años por la mayor experiencia del equipo quirúrgico y de los cuidados perioperatorios. El tiempo de estancia en UCI puede verse prolongado sin embargo el protocolo de extubación temprana ha reducido este tiempo a dos días en los últimos años. De la misma manera, el tiempo de estancia hospitalaria se ha reducido a 12 días.
Las complicaciones infecciosas fueron frecuentes con el 40% de los pacientes comprometidos, pero inferior a lo reportado en series tempranas de trasplante hepático donde el 60% de los individuos se infectaron 10, y comparables con los resultados actuales de grandes centros 11. De estas complicaciones, las infecciones bacterianas son las más frecuentes, se presentan especialmente durante los primeros dos meses y el origen más común fue el abdomen, seguido por el pulmón y el tracto urinario, información que coincide con los datos internacionales. Las infecciones virales y micóticas invasivas se presentaron en un porcentaje similar a lo reportado en otras series, incluso a pesar de que el protocolo de profilaxis antimicrobiana para citomegalovirus y hongos solo se aplica en pacientes con factores reconocidos de riesgo para las mismas 12,13.
En cuanto a las infecciones por micobacterias, se presentaron en el 0.8% de los pacientes, un dato relevante teniendo en cuenta la moderada prevalencia de esta enfermedad en Colombia 14, y acorde con otras series donde se esperan tasas de infección del 1 al 6% 15. La presentación clínica fue con enfermedad extrapulmonar, lo cual no es infrecuente en esta población y hace que el diagnóstico temprano sea más difícil.
Las complicaciones vasculares en general se presentaron en el 11% de los pacientes, con trombosis en la arteria hepática documentándose en el 3.7%, en todos los casos tempranas, un porcentaje similar a lo descrito por Duffy et al 16. Esta complicación continua siendo una de las más temidas en trasplante hepático ya que se relaciona con muerte en un 33% y pérdida del injerto en el 53% 17, como también se aprecia en esta serie donde el 50% falleció por falla orgánica múltiple y el 50% restante necesitó retrasplante hepático temprano o tardío a pesar de las medidas quirúrgicas o endovasculares.
En cuanto a las complicaciones en la vía biliar, estas se presentaron en el 14.5% de los pacientes, que concuerda con las estadísticas mundiales: 10-25% 18-21. Las estenosis anastomóticas fueron las lesiones más frecuentes en esta serie, estando relacionadas a incremento en las infecciones, procedimientos y hospitalizaciones, con lo cual aumentó los costos. Las fugas biliares se presentaron en una baja proporción, lo que está relacionado con el no uso del tubo en T biliar.
Los resultados de esta serie con respecto a rechazo agudo y crónico son similares a lo reportado recientemente por Pfitzmann et al., en Alemania, que encontraron un rechazo agudo y crónico en el 41% y 3.5% respectivamente 11 y por Boudjema et al., en Francia 22.
La cirrosis hepática por Hepatitis C es la principal causa de trasplante hepático en el mundo, sin embargo en nuestra serie solo fue del 12% evidenciando la baja prevalencia de la Hepatitis C en Colombia.
Las tasas de supervivencia de los pacientes con Carcinoma hepatocelular fueron similares a las de los otros pacientes de trasplante. Las tasas de recurrencia fueron menores al 10% similar a lo resportado en la literatura mundial cuando se cumplen los criterios de Milán 23.
En cuanto a las complicaciones a largo plazo como la insuficiencia renal crónica, la diabetes mellitus, la hipertensión arterial y la dislipidemia, las tasas fueron más bajas de lo reportado en la literatura, lo que podría explicarse por un tiempo de seguimiento más corto que el de otros registros en el mundo y por la dificultad en el control a largo plazo de algunos pacientes debido al sistema de salud local que permite cambiar el sitio de atención de los mismos.
La enfermedad hepática por alcohol fue la principal indicación para trasplante hepático en nuestra serie, similar a lo que es observado en otros países de Latinoamérica, sin embargo las tasas de recurrencia de alcohol fueron bajas (16.7%) y solamente 5.6% tuvieron recurrencia severa que llevaron a la disfunción del injerto hepático.
Existen solo cinco centros activos de trasplante hepático en Colombia y dos de ellos están localizados en Medellín. En nuestro país, las listas de espera de trasplante hepático son cortas debido a la alta tasa de donación de órganos, particularmente en nuestra región (32 por cada millón de habitantes), y la mortalidad en lista de espera es muy baja (menor del 5%). Este reporte es un buen ejemplo para otros centros de trasplante hepático en países en desarrollo con limitados recursos económicos, e.j. algunos centros en Asia y Latinoamérica, donde pueden ser obtenidos buenos resultados. Vale la pena mencionar la buena calidad de los donantes, particularmente en términos de edad y causa de muerte.
Como limitaciones de este estudio, se encuentra el seguimiento a largo plazo de algunos pacientes y el número limitado de casos porque se decidió analizar solo los pacientes con primer trasplante hepático y excluir la población de retrasplante, trasplante combinado higado-riñon y trasplante multivisceral por las características no comparables de estos grupos de pacientes.
Conclusión
En conclusión, el trasplante de hígado es una terapia efectiva y comprobada para las enfermedades hepáticas agudas y crónicas en pacientes seleccionados, a la cual ya se puede acceder en Colombia, con resultados en el Hospital Pablo Tobón Uribe de Medellín que son comparables tanto en supervivencia a mediano plazo como en complicaciones con los de otros centros del mundo.