Introducción
En el año 2006 la Asamblea General de las Naciones Unidas aprobó una resolución histórica que reconoce la amenaza global de la epidemia de diabetes. Por primera vez los gobiernos reconocieron que una enfermedad no infecciosa causa una amenaza a la salud mundial como la que representan enfermedades infecciosas, como el Sida, la TBC o la malaria. En Colombia entre un 7% y un 9% de la población adulta (20 años o más) tiene diabetes mellitus tipo 2 (DMT2), con una prevalencia cinco veces más baja en la zona rural 1. Con base en datos que se han recopilado en la última edición del Atlas de la Federación Internacional de diabetes (IDF) 2, se calcula que en el país hay más de 2 millones de personas con diabetes y la gran mayoría es la de tipo 2. Cerca del 50% de las personas desconocen su condición. En Colombia la Diabetes Mellitus es una de las cinco primeras causas de muerte y una de las 10 primeras causas de consulta en los adultos. Por consiguiente esta enfermedad constituye un problema de salud pública que debe ser manejado en todos los niveles de atención y con estrategias de prevención en todas sus etapas, para establecer el control de la diabetes en forma temprana y sostenida.
El control de la diabetes debe ser temprano, efectivo y sostenido para prevenir las complicaciones crónicas y evitar el efecto deletéreo de la memoria metabólica 3. Expertos sugieren utilizar niveles de la hemoglobina glicosilada (HbA1c) de 6.5% para el diagnóstico de diabetes y tomar este valor como punto de partida para su manejo. Los estudios clínicos controlados y aleatorizados como el UKPDS 4,5 han demostrado que si la DMT2 se trata adecuadamente desde un comienzo se puede reducir la incidencia de complicaciones crónicas atribuibles a la hiperglucemia prolongada. En particular se logró reducir el daño de la retina (retinopatía), del riñón (nefropatía) y del sistema nervioso periférico (neuropatía) al cabo de 10 años de una estrategia de manejo intensivo con insulina o sulfonilureas y se logró reducir la incidencia de infarto y la mortalidad con metformina. Con un seguimiento más largo hasta 20 años se demostró una reducción de eventos cardiovasculares fatales y no fatales con todos los antidiabéticos incluidos 5. La hemoglobina glicosilada (HbA1c) media asociada con estos beneficios fue en promedio de 7% y por lo tanto esta debe ser la meta del control glucémico. El tratamiento debe ser multifactorial porque es la estrategia más efectiva a mediano y largo plazo con la intención de controlar todos los factores de riesgo cardiovascular como la glucemia, los lípidos y la presión arterial 6,7.
Varios estudios han demostrado que la intervención de las personas con alto riesgo de desarrollar diabetes puede retardar su aparición y en varios países se están implementando estrategias de tamización con ese fin (Finlandia, por ejemplo). Eso permite también identificar a sujetos con una diabetes no reconocida que pueden beneficiarse del tratamiento e incluso reducir la incidencia de complicaciones 2. Existen ya escalas de riesgo que facilitan la tamización (por ejemplo, la FINDRISC) 8.
El manejo está lejos de ser sencillo y por el contrario, cada vez hay más medicamentos y dispositivos con probada eficacia y seguridad que ponen al médico en un dilema sobre cuándo y cómo formularlos y a qué pacientes. Es el médico de atención primaria quien debe tomar esta decisión en la mayoría de los casos. Además, siendo la diabetes una enfermedad crónica y progresiva que puede conducir a complicaciones, el médico debe trabajar con un equipo multidisciplinario que asegure la educación y adherencia del paciente y debe saber cuándo y cómo recurrir a especialistas. La tendencia actual a la individualización de las metas de manejo y de los tratamientos para lograrlas no se compadece con el alto volumen de pacientes y el tiempo limitado para atenderlos que tiene el médico de atención primaria. La OMS propone que se establezcan equipos compuestos por un médico entrenado en diabetes y una educadora en diabetes en el nivel de atención primaria, donde se debe atender a la gran mayoría de los pacientes con DMT2 no complicados. Todo paciente con DMT2 debe tener acceso a un programa estructurado de cambios del estilo de vida que le facilite al paciente llegar a tener un índice de masa corporal en el rango adecuado, una rutina de actividad física y un control sostenido de los factores de riesgo cardiovasculares, incluyendo el control glucémico 9.
El Ministerio de Salud y Protección Social encargó a la Pontificia Universidad Javeriana y a la Alianza de las Universidades Javeriana, Nacional y Antioquia (Alianza CINETS) el desarrollo de una Guía clínica sobre "El diagnóstico, tratamiento y seguimiento de la diabetes tipo 2 en la población mayor de 18 años". El presente documento proporciona recomendaciones, para la buena práctica, que están basadas en la mejor evidencia clínica disponible y las consideraciones adicionales relevantes para el contexto nacional como costos, preferencias de los pacientes y la relación entre los beneficios y riesgos de las tecnologías de interés.
Objetivos, alcance y población blanco de la guía
No se pretende presentar un compendio extenso de información clínica. Por el contrario se busca dar respuesta clara, concisa y sencilla a preguntas específicas que fueron seleccionadas por su importancia clínica, dando prioridad a los temas en que se consideró que aún existe una discusión entre los investigadores y entre los clínicos. También se incluyeron temas en los que se evidenció una variabilidad injustificada en las conductas realizadas en la práctica médica por los profesionales de salud en Colombia. Cabe aclarar que aquellos temas que son ampliamente aceptados en la literatura mundial y no ameritan por tanto un nuevo análisis de la literatura científica, se aceptaron como premisas a la presente guía, y como tal serán presentados en este documento.
Objetivo General. Brindar parámetros de la práctica clínica, basados en la mejor evidencia disponible, para la atención en salud y para la utilización racional de los recursos en el diagnóstico, tratamiento y seguimiento de la DMT2 en la población mayor de 18 años.
Objetivos específicos
• Determinar la utilidad, de estrategias de tamización como herramienta para la detección y diagnóstico temprano de la DMT2, en nuestro medio.
• Indicar las intervenciones farmacológicas dentro de un plan de manejo multifactorial, escalonado de menor a mayor complejidad, haciendo énfasis en la efectividad y seguridad, con miras a que sean aplicables a la mayoría de los pacientes DMT2 en atención primaria.
• Definir estrategias para la detección temprana de las complicaciones renales y cardiovasculares en los pacientes con DMT2.
Población blanco
Las recomendaciones van dirigidas a adultos mayores de 18 años en riesgo para el desarrollo de diabetes tipo 2 o con diagnóstico establecido de diabetes tipo 2.
A continuación se define cuáles son los tópicos que se abordarán y los que no se abordarán en la Guía.
En esta Guía NO se contemplan los siguientes temas:
• El manejo de pacientes en quienes se determine un alto riesgo de desarrollar diabetes durante el proceso de diagnóstico de la diabetes. Ej, los que resulten con glucemia de ayuno alterada y/o intolerancia a la glucosa y cuyo estado se ha identificado como una pre-diabetes.
• El manejo especifico de las complicaciones en pacientes con diagnóstico de diabetes mellitus, Ej, enfermedad renal crónica.
• El manejo especifico de la obesidad en el contexto de diabetes mellitus, entendiendo que si bien es fundamental el tratamiento de la misma, será abordado en una guía independiente.
Ámbito asistencial y población diana. Dada la importancia de esta patología, se hace necesario que las recomendaciones de la guías de práctica clínica se dirijan a todo el personal clínico asistencial que tenga a su cargo la detección temprana, atención integral y seguimiento de la diabetes tipo 2 en el adulto; en los diferentes niveles de atención. Esto incluye:
• Los médicos generales, de familia, internistas y en general toda la población médica que tiene como una de sus responsabilidades el tamizaje y manejo inicial, o la remisión del paciente con diabetes tipo 2.
• Los médicos especialistas en endocrinología y diabetes o que han realizado entrenamiento formal en diabetes.
• Personal del área de la salud que trabaja en clínicas de atención primaria de diabetes, así como los que trabajan en programas de educación en diabetes.
• Los especialistas en nutrición y nutrición clínica.
• El personal de las aseguradoras y prestadores de servicios de salud en sus programas de promoción y prevención, tamizaje y control de prevención primaria y secundaria de enfermedades cardio y cerebrovasculares.
• Los pacientes con diabetes tipo 2 o con alteraciones de la glucemia.
Materiales y Métodos
Esta guía de práctica clínica fue desarrollada por un grupo multidisciplinario de profesionales de la salud con experiencia y conocimiento en diferentes áreas (Médicos internistas con diferentes subespecialidades, endocrinólogos, médicos generales, médicos familiares, nutricionistas, enfermeras, psicólogas, educadores en diabetes) y representantes de los pacientes. Todos los integrantes del panel presentaron abiertamente la declaración de sus conflictos de interés. Estos documentos están disponibles en la versión completa de la guía (http://gpc.minsalud.gov.co/guias/Documents/diabetes/diabetes_tipo_2_completa.pdf).
El proceso de desarrollo de la guía se describe detalladamente en el manual para desarrollo de guías de práctica clínica y en la actualización de dicha metodología ( http://gpc.minsalud.gov.co/recursos/Documents/Guía%20Metodológica_Web.pdf). Dicho manual se generó con dos componentes fundamentales: Uno técnico, basado en el análisis de la mejor evidencia disponible, y uno participativo en el que múltiples grupos de expertos y de organizaciones interesadas hicieron su aporte para la generación del manual.
Cabe resaltar que dicha metodología garantizó una búsqueda sistemática de la evidencia científica (incluyendo tanto revisiones sistemáticas de la literatura como estudios primarios). Así mismo estableció una metodología transparente para la selección de la mejor evidencia a utilizar, y para una evaluación cuidadosa de la calidad. La versión completa de la presente guía, en la que se presentan los resultados de todas estas evaluaciones, pueden ser consultada en http://gpc.minsalud.gov.co/Pages/Default.aspx. El grupo metodológico preparó un resumen de la evidencia disponible y lo presentó al panel completo durante las reuniones de generación de las recomendaciones.
La calidad del conjunto de la evidencia que sirvió como base para la formulación de las recomendaciones fue evaluada utilizando el sistema GRADE aplicado a las revisiones sistemáticas, experimentos clínicos aleatorizados o estudios observacionales incluidos. Para el sistema GRADE, la calidad de la evidencia se asigna a cada desenlace definido como crítico para obtener posteriormente una calificación global del cuerpo de la evidencia para cada comparación en estudio.
La calidad de la evidencia depende de los siguientes factores: riesgo de sesgo, inconsistencia, presencia de evidencia directa o indirecta, imprecisión y riesgo de sesgo de publicación, además de la magnitud del efecto, la presencia de un gradiente dosis - respuesta y la acción de potenciales factores de confusión residuales.
Para la presentación de la calidad de la evidencia y el resumen de los hallazgos se utilizaron perfiles de evidencia GRADE que fueron producidos utilizando el programa GRADEpro a través de GDT: Guideline Development Tool. Las posibles calificaciones de la evidencia con su significado e interpretación gráfica se presentan en la Tabla 1.
| Nivel de evidencia | Definición | Representación gráfica |
|---|---|---|
| Alta | Se tiene gran confianza en que el verdadero efecto se encuentra cerca al estimativo del efecto | ⴲ ⴲ ⴲ ⴲ |
| Moderada | Se tiene una confianza moderada en el estimativo del efecto: es probable que el verdadero efecto esté cercano al estimativo del efecto, pero existe la posibilidad de que sea sustancialmente diferente | ⴲ ⴲ ⴲ ⴱ |
| Baja | La confianza que se tiene en el estimativo del efecto es limitada: el verdadero efecto puede ser sustancialmente diferente del estimativo del efecto | ⴲ ⴲ ⴱ ⴱ |
| Muy baja | Se tiene muy poca confianza en el estimativo del efecto: es probable que el verdadero efecto sea sustancialmente diferente del estimativo del efecto | ⴲ ⴱⴱ ⴱ |
| Fuente: Guía Metodológica para la elaboración de Guías de Práctica Clínica con Evaluación Económica en el Sistema General de Seguridad Social en Salud Colombiano 10 | ||
La fuerza asignada a cada recomendación, de acuerdo con el sistema GRADE, se basó tanto en la calidad de la evidencia subyacente, como en la información y juicio de los pacientes y los expertos acerca del balance entre los riesgos y los beneficios de las alternativas recomendadas, la coherencia de las recomendaciones con los valores y preferencias de los pacientes, la disponibilidad y aplicabilidad local de las tecnologías o alternativas y la utilización de recursos y costos asociados a la implementación de las recomendaciones.
La forma en que deben interpretarse estas recomendaciones para médicos y pacientes se presenta en la Tabla 2.
| Grupo de usuarios | Recomendación fuerte | Recomendación débil |
|---|---|---|
| Pacientes | La gran mayoría de las personas en su situación querrán el curso de acción recomendado y solo una pequeña proporción no querrá utilizarla | Una parte importante de las personas en su situación querrán utilizar el curso de acción recomendado, pero muchas no querrán utilizarla |
| Clínicos | La mayoría de los pacientes deberían recibir el curso de acción recomendado | Reconozca que diferentes opciones pueden ser apropiadas para diferentes pacientes y debe hacer un esfuerzo adicional para ayudar al paciente a tomar decisiones de manejo consistentes con sus propios valores y preferencias; las ayudas para la toma de decisiones y la toma de decisiones compartidas pueden ser particularmente útiles |
| Trazadores de políticas | La recomendación puede ser adoptada como política en la mayoría de las situaciones | La formulación de políticas requiere debate y participación de varios grupos de interés |
| Fuente: traducido del manual de GRADE Profiler (Disponible a través de la página electrónica www.who.int/hiv/topics/mtct/grade_handbook.pdf) | ||
La versión final de la Guía fue evaluada por pares internacionales, seleccionados por el Ministerio de Salud y Protección Social, expertos tanto en diabetes como en metodología. Sus aportes fueron tenidos en cuenta por el grupo desarrollador de la guía.
Recomendaciones
Tema 1. Tamización y diagnóstico de la diabetes mellitus tipo 2
Premisas. El Diagnóstico de la diabetes mellitus tipo 2 se puede hacer con cualquiera de los siguientes criterios:
• Glucemia plasmática en ayunas ≥ 126 mg/dL
• Glucemia plasmática ≥200 mg/dL a las dos horas de tomar una carga de 75 g de glucosa anhidra disuelta en agua. Esta es una prueba de tolerancia oral a la glucosa (PTOG).
• HbA1c en cualquier momento ≥6.5%
• En presencia de síntomas (poliuria, polidipsia y pérdida de peso) basta con una glucemia plasmática al azar ≥200 mg/dL para establecer el diagnóstico.
Pregunta clínica 1. ¿Debería utilizarse el FINDRISC como una prueba adecuada para tamización de diabetes no diagnosticada, en población Colombiana adulta?.
Respuesta a la pregunta. El enfoque ideal sería un estudio en el que a un grupo se le haga la tamización con la aplicación del test de FINDRISC para luego realizar pruebas sanguíneas confirmatorias de acuerdo a los resultados y dar tratamiento a quienes resulten positivos en estas pruebas confirmatorias, y compararlo con otro grupo al que se le haga tamización con pruebas sanguíneas y se le de tratamiento a quienes tengan resultados positivos confirmatorios. Se debería incluir un tercer grupo al que no se haría tamización y solo se le daría tratamiento a quienes sean detectados por evolución clínica.
Desafortunadamente no existe ningún estudio de este tipo, por lo que se presenta inicialmente la información de estudios que comparan el tamizaje mediante pruebas sanguíneas con la detección por evolución clínica. Posteriormente se presenta información que comparó la tamización mediante pruebas sanguíneas con la tamización basada en el test de FINDRISC, y por último se hace a una aproximación con respecto al potencial efecto de los resultados de este tamizaje en los desenlaces críticos para los pacientes, asumiendo que reciben tratamiento aquellos que resultan positivos en la tamización.
Un estudio realizado en el Reino Unido 11 comparó tres grupos tomados de una cohorte poblacional de sujetos entre 40 y 65 años de edad: en una primera etapa (1990-1992), un tercio de la población escogida al azar fue invitada a realizarse la tamización con una prueba de tolerancia oral a la glucosa (PTOG) y con la documentación de factores de riesgo cardiovascular. Lo mismo se hizo 10 años después en una segunda etapa (2000-2003) con la mitad de los que no se seleccionaron inicialmente y que seguían vivos; el resto nunca se invitó a la tamización. Los resultados de las pruebas se informaron a los médicos generales para que tomaran las medidas que consideraran convenientes. En la primera etapa, los sujetos que acudieron a la invitación para realizar el tamizaje tuvieron menor mortalidad al cabo de 10 años de seguimiento comparados con los que no fueron invitados (HR= 0.54; IC 95%= 0.40-0.74), mientras que los que fueron invitados y no acudieron tuvieron mayor mortalidad en el mismo período (HR= 1.36; IC 95% = 1.01-1.82 vs. no invitados). En la segunda etapa al cabo de 8 años de seguimiento también tuvieron una menor mortalidad los que aceptaron la tamización al compararlos con los que no fueron invitados (HR= 0.52; IC 95%= 0.35-0.78) mientras los que fueron invitados y no acudieron tuvieron la mayor mortalidad (HR= 1.73; IC 95%= 1.34-2.24 vs. no invitados). Este estudio nos permite concluir que la invitación para realizar el tamizaje de diabetes mellitus no es suficiente, este debe realizarse efectivamente para lograr una disminución en la mortalidad a largo plazo.
El test FINDRISC fue construido a partir de los datos de una cohorte poblacional finlandesa de sujetos entre 35 y 64 años seleccionados al azar en 1987 y seguidos por 10 años, con el fin de predecir el desarrollo de una diabetes tratada con medicamentos. Fue validada con otra cohorte independiente seleccionada al azar en 1992 y seguida por 5 años 12. El puntaje del FINDRISC varíó entre 0 y 20 puntos y un valor mayor o igual a 9 puntos predijo diabetes con una sensibilidad de 0.78 y 0.81, especificidad de 0.77 y 0.76 y valor predictivo positivo de 0.13 y 0.05 en las cohortes de 1987 y 1992 respectivamente.
El FINDRISC ha sido validado en otras poblaciones. En Bulgaria se seleccionaron sujetos con al menos un factor de riesgo mayor para diabetes; un puntaje del FINDRISC mayor o igual a 12 demostró una sensibilidad de 0.78 (IC 95%= 0.73-0.85) y especificidad de 0.62 (IC 95%= 0.58-0.68) para identificar sujetos con diabetes o pre-diabetes 3. En Grecia se validó en una muestra poblacional y un puntaje igual o mayor a 15, tuvo una sensibilidad de 0.82 y una especificidad de 0.60 para predecir la presencia de diabetes desconocida. El área bajo la curva ROC fue de 0.72 para detectar diabetes y de 0.72 para cualquier grado de disglucemia 13. También se validóado en España donde el área bajo la curva ROC para detectar DMT2 no diagnosticada fue de 0.74 y para predecir DMT2 incidente fue de 0.75. El puntaje que tuvo mayor valor predictivo fue igual o mayor a 9 en presencia de una glucemia en ayunas mayor a 100 mg/dL 14.
Aunque existen varias escalas similares al FINRISC, esta es quizás la más utilizada a nivel mundial y la más apropiada para usar en nuestra población 15.
En Colombia se validó un FINRISC modificado para ajustar los puntos de corte de la circunferencia de cintura a las medidas apropiadas para diagnosticar obesidad abdominal en la población latinoamericana (94 cm en hombres y 90 cm en mujeres) 16, con lo cual se obtuvo una sensibilidad del 74% y una especificidad del 60% para detectar cualquier alteración en la regulación de la glucosa (diabetes o pre-diabetes) con un puntaje igual o mayor a 12 en una población de voluntarios sin diagnóstico de diabetes 17.
Estos valores sugieren que es baja la cantidad de falsos negativos y según la información disponible en la literatura, estos pacientes presentarán una muy baja tasa de complicaciones en los siguientes tres años 18, momento en el cual se llevarán nuevamente a tamización. Los falsos positivos no representarán un impacto significativo sobre el estado emocional (ansiedad o depresión) de los pacientes 19.
Una vez aplicada la prueba y habiéndose documentado el FINDRISC alto (punto de corte de 12) se mediría la glicemia en ayunas como primera prueba diagnóstica, para proseguir según su resultado en el proceso diagnóstico. En caso tal de que no se documente DMT2 y con el simple hecho de ser aplicado el cuestionario de tamización, se garantizaría para el paciente la primera fase de educación acerca de los buenos hábitos de vida, lo cual resultaría beneficioso para la población. Se anota en la discusión para emitir las recomendaciones de la guía, que si bien el FINDRISC se establece como estrategia autoaplicable, la replicabilidad y validez de las mediciones de masa corporal y del perímetro abdominal son mayores cuando los realiza un profesional capacitado, por lo que es preferible que sea aplicado por este último.
El grupo desarrollador de la presente guía hizo adicionalmente una evaluación económica para determinar cuál era la estrategia de tamización más adecuada en Colombia 20. Dicha evaluación comparó esquemas que iniciaban con la realización de la prueba de glucosa en ayunas, con esquemas que iniciaban con la realización del cuestionario FINDRISC. La estrategia de tamización que incluyó FINDRISC, más la realización de la prueba de glucosa en ayunas en pacientes con puntaje superior a 12, complementada con la realización de la prueba de tolerancia oral a la glucosa para aquellos pacientes con reporte de glicemia entre 100 y 125 mg/dL, fue la estrategia que resultó más costo-efectiva en Colombia, lo que apoya la recomendación de utilizar el FINDRISC en nuestro medio.
Recomendaciones
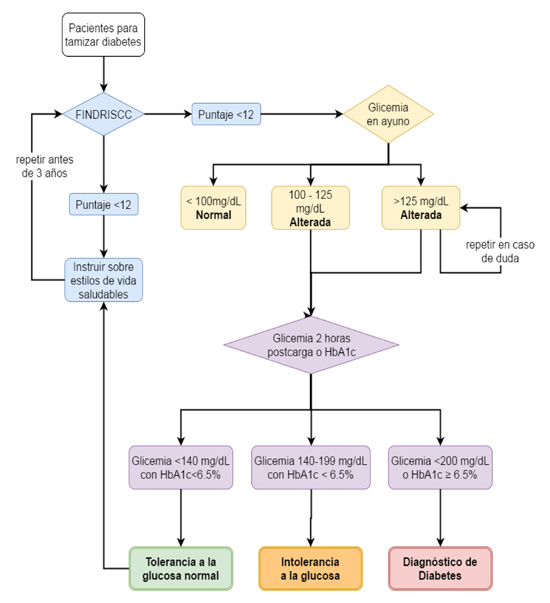
1. Se recomienda el uso del FINDRISC (estableciendo el punto de corte en 12), como método de tamización de DMT2 en adultos en Colombia ( Fig. 1 )
Figura 1.
Algoritmo para tamización y diagnóstico de DMT2.
DMT2: diabetes mellitus tipo 2, FINDRISCC: FINnish Diabetes Risk Score, HbA1c: hemoglobina glicosilada
Recomendación fuerte a favor. Calidad de la evidencia moderada ⴲ ⴲ ⴲⴱ
Puntos de buena práctica clínica
✔ El FINDRISC debe ser aplicado por personal familiarizado con la herramienta. En el Anexo 1 se ilustra el cuestionario FINDRISC adaptado a la población colombiana
✔ Se debe realizar una prueba diagnóstica de la diabetes mellitus a todas las personas que tengan un puntaje ≥12 en el FINDRISC.
✔ La prueba diagnóstica más apropiada es la medición de una glucemia plasmática en ayunas
✔ Si es la preferencia del paciente, puede realizarse glucemia plasmática en ayuno como prueba inicial de tamización y diagnóstico de la diabetes mellitus.
✔ En las personas con un puntaje ≥12 en el FINDRISC que no cumplan criterios diagnóstico de la diabetes mellitus, se recomienda establecer la presencia de categorías con riesgo aumentado de diabetes (Prediabetes)* para incluirlos en programas de prevención de DMT2.
*Categorías con riesgo aumentado de diabetes:
- Glucemia de ayuno alterada: Glucemia plasmática en ayunas entre 100 y 125 mg/dL
- Intolerancia a la glucosa: Glucemia plasmática a las 2 h entre 140 y 199 mg/dL en una PTOG.
✔ En todos los casos debe hacerse educación sobre estilos de vida saludable, enfatizando en el control de los factores de riesgo para DM que fueron identificados con la escala.
✔ A las personas con puntaje menor a 12 en el FINDRISC, se les debe instruir sobre la importancia de estilos de vida saludable y realizar nuevo tamización a los tres años.
Pregunta clínica 2. ¿Debe utilizarse la hemoglobina glicosilada (HbA1c) para sustituir a la prueba de tolerancia oral a la glucosa (PTOG), para el diagnóstico de diabetes?
Respuesta a la pregunta. Un meta-análisis que comparó la capacidad diagnóstica de la HbA1c con la de la prueba de tolerancia oral a la glucosa (PTOG) como la prueba de referencia 21 demostró que la HbA1c es una herramienta adecuada para confirmar el diagnóstico de diabetes mellitus. En los pacientes que mostraron positividad con una herramienta de tamizaje, la HbA1c dada su alta especificidad (95.6%), permitió descartar razonablemente el diagnostico en pacientes que no tienen la enfermedad.
La mayor limitante de la HbA1c se debe a la presencia de una sensibilidad intermedia, de solo el 51.8%, lo cual llevaría a que un porcentaje significativo de pacientes con diabetes mellitus no sean detectados por esta prueba. Se consideró que si el paciente tenía un riesgo muy alto de diabetes en la prueba de tamizaje, se deberá realizar una prueba de tolerancia oral a la glucosa en caso de que la HbA1c resulte menor de 6.5%.
Con la evidencia mencionada se aplicó la metodología GRADE 22 para preguntas de pruebas diagnósticas, evaluando el potencial impacto de los resultados de la prueba en los desenlaces finales de los pacientes que fueron clasificados erróneamente como falsos positivos (ansiedad, depresión) y falsos negativos (mortalidad y complicaciones macro y microvasculares). Como se explicó en la pregunta clínica 1, no se encontró un impacto significativo sobre ansiedad o depresión en los pacientes falsos positivos. Con base en los datos reportados por los estudios UKPDS 23 y ADDITION 18, se encontró que el impacto a tres años de un diagnóstico inadecuado no fue significativo, encontrando tasas similares de muerte y complicaciones micro y macrovasculares entre pacientes mal diagnosticados, y los pacientes que fueron diagnosticados correctamente y recibieron manejo farmacológico. Se tuvo en cuenta el impacto a tres años, asumiendo que a estos pacientes se les seguirá realizando tamizaje con al menos este intervalo de tiempo.
En la evaluación económica para determinar cuál era la estrategia de tamización más adecuada en Colombia que se describió en la pregunta 1 se comparó la medición de la glucemia 2h post-carga de glucosa (PTOG) con la medición de la HbA1c como método diagnóstico de DM en los casos con puntaje alto en el FINDRISC y glucemia de ayuno alterada. En esa secuencia diagnóstica, la PTOG y no la HbA1c fue la estrategia que resultó más costo efectiva en Colombia 20. Sin embargo la HbA1c es fundamental para decidir el tratamiento inicial y debe realizarse a todos los sujetos que resulten con el diagnóstico de DM (como se verá más adelante), por lo cual su costo-efectividad podría cambiar cuando la probabilidad de tener DM es muy alta.
Recomendaciones (Fig. 1)
2. Se sugiere utilizar la hemoglobina glicosilada (HbA1c) como estrategia para diagnosticar diabetes mellitus en pacientes con glucemia plasmática en ayunas entre 100 y 125 mg/dL. También se puede utilizar para corroborar el diagnóstico cuando el resultado de la glucemia plasmática en ayunas es equívoco*. Un valor ≥6.5% confirma el diagnóstico.
Recomendación débil a favor de su uso. Calidad de la evidencia baja ⴲ ⴲ ⴱⴱ
3. Se sugiere utilizar la prueba de tolerancia oral a la glucosa (PTOG) como estrategia para el diagnóstico de la diabetes mellitus en pacientes con glucemia plasmática en ayunas entre 100 y 125 mg/dL que manifiesten su preferencia por esta estrategia. También se puede utilizar para corroborar el diagnóstico cuando el resultado de la glucemia plasmática en ayunas es equívoco*. Un valor ≥200 mg/dL a las 2 h de ingerir una carga de 75 g de glucosa confirma el diagnóstico ( Fig. 1 ).
Recomendación débil a favor de su uso. Calidad de la evidencia alta ⴲ ⴲ ⴲ ⴲ
*Se considera glucemia plasmática en ayunas equivoca cuando las dos mediciones de glicemia son divergentes, es decir una es mayor de 125 y la otra menor
Puntos de buena práctica clínica
✔ Los laboratorios que realizan la prueba de HbA1c deberán cumplir con las normas internacionales, garantizando que los kits utilizados y sus respectivos métodos sean certificados por la NGSP (National Glycohemoglobin Standardization Program - www.ngsp.org).
✔ En caso que la sospecha clínica de diabetes mellitus sea alta en la prueba de tamización y la HbA1c se encuentre por debajo de 6.5%, se deberá realizar una prueba de tolerancia oral a la glucosa (PTOG) para confirmar el diagnóstico o para establecer la presencia de categorías con riesgo aumentado de diabetes (Prediabetes)* para incluirlos en programas de prevención de DMT2.
*Categorías con riesgo aumentado de diabetes:
- Glucemia de ayuno alterada: Glucemia plasmática ayuno entre 100 y 125 mg/dL
- Intolerancia a la glucosa: Glucemia a las 2 h entre 140 y 199 mg/dL en una PTOG
✔ La prueba PTOG detecta más casos de diabetes que la HbA1c y por consiguiente resulta ser más costo efectiva. Se debe utilizar cuando se desea diagnosticar al mayor número de personas que tienen diabetes.
✔ En todos los casos en que se diagnostique diabetes mellitus, se debe medir la HbA1c al comienzo para utilizarla en la toma de decisiones sobre el tratamiento a seguir y para poder evaluar posteriormente el efecto del tratamiento (ver pregunta clínica 4).
✔ En todos los casos en los que se descarte el diagnóstico de diabetes mellitus debe hacerse educación sobre estilos de vida saludable, enfatizando en el control de los factores de riesgo para diabetes mellitus que fueron identificados inicialmente en tamización.
Tema 2. Manejo inicial de la diabetes tipo 2
Premisas. El objetivo fundamental del tratamiento consiste en lograr cambios intensivos en el estilo de vida que conduzcan a un control metabólico permanente mediante la normalización y mantenimiento del peso y el incremento persistente de la actividad física.
La dieta debe ser fraccionada y balanceada, teniendo en cuenta la edad y la actividad del sujeto.
Se debe reducir el consumo de alimentos fuentes de carbohidratos simples y de grasas saturadas y trans, que se pueden sustituir por grasas provenientes de pescados y de aceites vegetales, preferiblemente de predominio monoinsaturado como el de canola y el de oliva.
Se debe aumentar el consumo de frutas enteras y verduras como fuentes de fibra y antioxidantes. También el de leguminosas como fuente de proteína y fibra, siempre y cuando se tenga en cuenta su mayor contenido calórico.
El manejo de los pacientes con DMT2 debe ser multifactorial para lograr un control adecuado de todos los factores de riesgo cardiovasculares como la hiperglucemia, la dislipidemia, la hipertensión arterial y el tabaquismo.
Todo paciente con DMT2 debe ingresar a un programa educativo que lo apoye para que modifique su estilo de vida, alcance los objetivos terapéuticos y prevenga las complicaciones de la diabetes.
El programa educativo debe ser continuo y debe estar liderado por un profesional de la salud certificado en educación diabetológica, con el apoyo de profesionales en otras áreas de la salud como nutrición, enfermería, educación física, psicología, podología y odontología.
El tratamiento farmacológico se comienza usualmente con antidiabéticos orales cuando el paciente está clínicamente estable, aunque tenga una HbA1c muy elevada. El descenso de la HbA1c es directamente proporcional al grado de elevación inicial de la misma.
Cuando el paciente se encuentra muy sintomático y clínicamente inestable, con pérdida aguda de peso, signos de deshidratación, evidencia de cetosis y glucemias muy elevadas, se recomienda iniciar insulina aunque luego se pueda retirar gradualmente.
La persona con DMT2 y exceso de peso debe entrar a un programa que le ayude a hacer una dieta con la reducción de ingesta calórica necesaria para perder peso y alcanzar un índice de masa corporal cercano a 25 kg/m².
El empleo inicial concomitante de medicamentos aprobados para reducción de peso, incluyendo algunos antidiabéticos como los agonistas del receptor de GLP-1, puede estar indicado en pacientes con DTM2 y obesidad (IMC ≥30 kg/m²)
Cuando el paciente con DMT2 tiene una obesidad mórbida, con un IMC ≥35 kg/m², se puede beneficiar si ingresa a un programa dirigido a practicarle una cirugía bariátrica en caso de que reúna los criterios a favor, no tenga contraindicaciones y demuestre estar dispuesto a cambiar intensivamente su estilo de vida.
Pregunta clínica 3. ¿En personas adultas con diabetes mellitus tipo 2 (DMT2) recién diagnosticada, se puede iniciar manejo solamente con cambios intensivos de estilo de vida?
Respuesta a la pregunta: El UKPDS ha sido el estudio más grande y de mayor seguimiento en personas con DMT2 y se diseñó para establecer la efectividad del control glucémico intensivo inicial sobre las complicaciones de la diabetes 5. El manejo intensivo se inició con sulfonilurea o insulina basal y el convencional solamente con dieta. A pesar de que el control glucémico se deterioró en ambos grupo, se logró mantener una diferencia de HbA1c de 0.9% y el grupo intensivo mantuvo una mediana de HbA1c de 7%, con lo cual se redujo significativamente la incidencia de cualquier complicación relacionada con la diabetes y en particular la incidencia de complicaciones microvasculares. En un subgrupo de pacientes con sobrepeso se inició el manejo intensivo con metformina, y a pesar de que mantuvo una mediana de HbA1c un poco más alta (7.4%) y de que la diferencia con el grupo control fue apenas de 0.6%, este grupo tuvo la mayor reducción de la incidencia de cualquier complicación relacionada con la diabetes y una reducción significativa de mortalidad. El peso en ese grupo de pacientes se mantuvo muy similar al del grupo control 24. A partir de estos resultados, las guías de práctica clínica vienen proponiendo que se inicie el tratamiento intensivo de la DMT2 con cambios de estilo de vida y preferiblemente con metformina.
Un estudio reciente de alta calidad metodológica determinó el impacto de una intervención multifactorial dirigida a perder peso con dieta y ejercicio intensivos, comparada con apoyo y educación diabetológica, en pacientes con DMT2 durante una mediana de cinco años 25. A pesar de que lograron perder 8.6% del peso corporal al cabo del primer año y 6% al final del estudio (vs. 0.7 y 3.5% en el grupo control) y de un leve cambio en la HbA1c, no se logró una reducción significativa de la incidencia de eventos cardiovasculares fatales o no fatales y el estudio se suspendió prematuramente por los resultados del análisis de futilidad. Es importante anotar que los beneficios iniciales del cambio intensivo del estilo de vida como pérdida de peso y disminución de la HbA1c) comenzaron a perderse a partir del primer año de intervención.
Ya evaluando de forma individual el impacto de cada uno de los cambios de estilo de vida, la evidencia demuestra que la actividad física tiene un impacto favorable sobre el riesgo de morir. En una cohorte de sujetos con DMT2 seguidos por un promedio de 9.4 años 26 se demostró una tendencia significativa a reducir el riesgo de mortalidad total y cardiovascular con mayores niveles de actividad física total medida por una escala y con mayor intensidad de actividad física durante el tiempo de ocio medida en mets-h/semana, pero no con mayor tiempo de caminata. El menor riesgo de mortalidad total (HR= 0.62, IC 95%= 0.49-0.78) y cardiovascular (HR= 0.51; IC 95%= 0.32-0.81) se observó en las personas moderadamente activas. En un meta-análisis de cinco estudios incluyendo el anterior, el riesgo de morir por cualquier causa fue menor para la actividad física total alta vs. baja (HR= 0.60; IC 95%= 0.49-0.73). Los programas de ejercicio estructurados tienen un mayor impacto sobre el control glucémico al compararlos con la sola recomendación de realizar actividad física, (Reducción de HbA1c= -0.73%; IC 95%= -1.06%- -0.40% vs. -0.57%; IC 95%= -1.14%- -0.01% respectivamente) 27. El efecto se observó tanto con el ejercicio aeróbico como con el de resistencia y la combinación de ambos tipos de ejercicio produjo un impacto similar. Adicionalmente este impacto es mayor en la medida que aumentó el número de sesiones semanales, demostrándose una disminución adicional de la HbA1c de -0.39% por cada sesión de ejercicio.
En lo referente a la evaluación de intervenciones nutricionales estructuradas, un meta-análisis reciente de 16 estudios con seguimientos entre 6 meses y 4 años demostró que las dietas bajas en carbohidratos, con bajo índice glucémico, con alto contenido proteico o del tipo mediterráneo, todas mejoran significativamente el control glucémico vs. el grupo comparador, pero la dieta mediterránea produjo el mayor descenso de la HbA1c (-0.47% en promedio, p= <0.00001) y la mayor pérdida de peso (-1.84 kg en promedio, p= <0.00001 ) 28. Adicionalmente un estudio clínico controlado y aleatorizado de buena calidad demostró que la dieta mediterránea redujó significativamente el riesgo de eventos cardiovasculares mayores (infarto agudo de miocardio, ataque cerebrovascular o muerte por causa cardiovascular) (HR= 0.70; IC 95%= 0.54-0.92), en sujetos con alto riesgo cardiovascular seguidos por un promedio de 4.8 años. Casi la mitad tenían diabetes y no se demostró interacción por tener o no esta condición en el análisis de subgrupos 29.
Conociendo esta información se consideró al interior del grupo desarrollador de la guía que la evidencia a favor de iniciar un manejo con cambios intensivos del estilo de vida, como manejo único en pacientes con diabetes mellitus 2 recién diagnosticada, era insuficiente. Adicionalmente se tuvo en cuenta que existe información de buena calidad que ha demostrado que iniciar un manejo farmacológico con metformina en pacientes con diabetes mellitus tipo 2 recién diagnosticada, ayuda a disminuir desenlaces cardiovasculares a largo plazo.
Así mismo se consideró que la evidencia disponible era suficiente para demostrar beneficios clínicos para los pacientes al combinar desde un comienzo el manejo farmacológico con los cambios terapéuticos del estilo de vida.
Recomendaciones (Fig. 2)
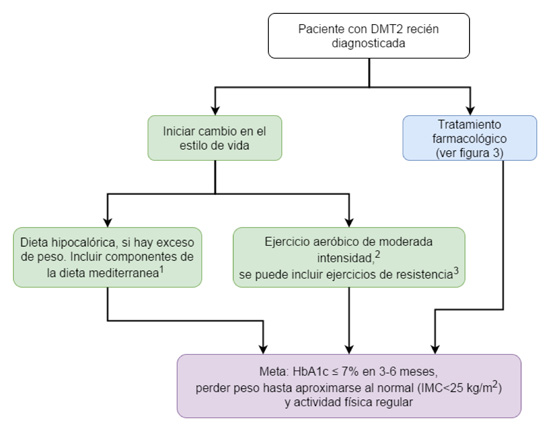
Figura 2
Algoritmo para el manejo inicial de pacientes con DMT2.
1 La dieta mediterránea adaptada a nuestro medio debe incluir el consumo, principalmente, de vegetales, hortalizas, legumbres, cereales integrales, frutas enteras, frutos secos y aceite de oliva o de nueces; también, el consumo moderado de pescado, aves y productos lácteos bajos en grasa. El consumo de carnes rojas, huevos, granos refinados y azúcares debe ser esporádico.
2Los ejercicios aeróbicos: incluyen actividades como montar en bicicleta, caminar, nadar, bailar y hacer movimientos rítmicos repetidos (≥10) de un mismo grupo muscular. La frecuencia debe ser ≥150 min por semana, y la intensidad no debe exceder una frecuencia cardiaca equivalente a (220−edad) × 0.7.
3 Los ejercicios de resistencia incluyen la rutina con pesas, que debe ser gradual en la cantidad de peso y en la frecuencia.
DMT2: diabetes mellitus tipo 2, HbA1c: hemoglobina glicosilada, IMC: índice de masa corporal
4. En los pacientes con DMT2 recién diagnosticada no se recomienda como tratamiento inicial el manejo únicamente con cambios en el estilo de vida
Recomendación fuerte en contra de la intervención. Calidad de la evidencia moderada ⴲ ⴲ ⴲ ⴱ
5. En los pacientes con DMT2 recién diagnosticada se recomienda iniciar el tratamiento farmacológico con metformina de forma simultánea con los cambios en el estilo de vida, aunque el valor inicial de HbA1c esté cercano a la meta
Recomendación fuerte a favor de la intervención. Calidad de la evidencia moderada ⴲ ⴲ ⴲ ⴱ
6. En los pacientes con DMT2 recién diagnosticada se sugiere que los cambios en el estilo de vida incluyan los componentes de la dieta mediterránea
Recomendación débil a favor. Calidad de la evidencia moderada ⴲ ⴲ ⴲ ⴱ
7. En los pacientes con DMT2 recién diagnosticada se sugiere que los cambios en el estilo de vida incluyan ejercicio aeróbico de moderada intensidad.
Recomendación débil a favor. Calidad de la evidencia baja ⴲ ⴲ ⴱⴱ
8. En los pacientes con DMT2 recién diagnosticada se sugiere que los cambios en el estilo de vida incluyan ejercicio de resistencia, en los casos en los que se haga manifiesta dicha preferencia.
Recomendación débil a favor. Calidad de la evidencia muy baja ⴲ ⴱⴱⴱ
Puntos de buena práctica clínica
Cuando se inicie el cambio de estilo de vida se debe tener en cuenta los siguientes elementos:
✔ Se recomienda adaptar la dieta mediterránea a las características del medio, pero conservando el predominio del consumo de vegetales, hortalizas, legumbres, cereales integrales, frutas enteras, frutos secos y aceite de oliva o nueces. Incluye consumo moderado de pescado, aves, productos lácteos bajos en grasa y vino con las comidas si forma parte del hábito del paciente. El consumo de carnes rojas, huevos y granos refinados debe ser esporádico.
✔ El consumo habitual de alcohol no se debe estimular.
✔ Se debe establecer un programa estructurado de ejercicio para que éste tenga un impacto favorable
✔ El ejercicio aeróbico incluye actividades como montar en bicicleta, caminar, nadar, bailar y movimientos rítmicos repetidos (≥10) de un mismo grupo muscular. La frecuencia debe ser igual o mayor a 150 min por semana y la intensidad no debe exceder una frecuencia cardíaca equivalente a (220 - edad) x 0.7. Para que tenga efecto reductor de peso, el ejercicio debe ser mucho más frecuente.
✔ El ejercicio de resistencia incluye rutina con pesas que debe ser gradual en la cantidad de peso y la frecuencia.
✔ Se sugiere, en pacientes con DMT2 recién diagnosticada que tengan limitaciones físicas que le impidan la movilidad, individualizar la prescripción de ejercicio y que sea valorado por un fisiatra o un médico del deporte.
✔ Si el paciente está clínicamente inestable es preferible aplazar el comienzo del ejercicio hasta que esté compensado.
✔ La metformina debe dosificarse en forma gradual partiendo de 500 mg al día hasta llegar a 1000 mg dos veces al día para evitar intolerancia gastrointestinal (náuseas, dolor abdominal, diarrea). Si hay intolerancia gastrointestinal, puede minimizarse tomándola después de las comidas y utilizando la presentación de liberación prolongada.
✔ Se debe reducir la dosis de metformina a un máximo de 1000 mg al día cuando la tasa de filtración glomerular esté por debajo de 50 mL/min y se debe suspender cuando esté por debajo de 30 mL/min. Está contraindicada también cuando hay un riesgo alto de acidosis láctica, como en estados de hipoxemia severa, falla hepática y alcoholismo.
✔ Cuando la metformina está contraindicada o no se tolera, se puede reemplazar como tratamiento inicial por cualquiera de los otros antidiabéticos orales que esté aprobado para monoterapia.
Pregunta clínica 4. ¿En personas adultas con diabetes mellitus tipo 2 recién diagnosticada, cuándo se debe iniciar un manejo con más de un medicamento para obtener un control glucémico adecuado?
Respuesta a la pregunta. Al evaluar la evidencia disponible sobre la combinación de medicamentos como manejo farmacológico inicial en pacientes con DMT2, todos los medicamentos evaluados presentan disminuciones de HbA1c significativas y de similar magnitud al ser combinados con metformina como terapia inicial (Reducción HbA1c= -0.43%; IC 95%= -0.56--0.30) 30. De igual forma todos los antidiabéticos orales aumentan de forma significativa la probabilidad de alcanzar metas de control glucémico (RR para alcanzar HbA1c <7%= 1.40; IC 95%= 1.33-1.48) 30.
Cabe resaltar que ninguna de las terapias combinadas tiene evidencia que sugiera un impacto en el riesgo de complicaciones microvasculares y la evidencia del impacto sobre el riesgo cardiovascular es débil.
De acuerdo con esta información se consideró al interior del grupo desarrollador de la guía que existe suficiente evidencia a favor de iniciar manejo farmacológico con terapia combinada desde el inicio en pacientes con DMT2 recién diagnosticada para obtener un mejor control metabólico. Se sugiere hacerlo cuando al momento del diagnóstico el valor de HbA1c es mayor del 8%, por ser éste el valor promedio mínimo de los pacientes incluidos en esos estudios y porque se encuentran a más de un punto de la meta del 7%, que es lo que suele reducir el tratamiento con metformina como monoterapia.
Dada la similitud en la eficacia de los diferentes medicamentos, se considera fundamental evaluar los riesgos de efectos adversos para definir el medicamento que se va a combinar con metformina. El riesgo de hipoglucemia aumentó significativamente cuando se compararon las combinaciones iniciales de metformina con la metformina sola (RR= 1.56; IC 95%= 1.08-2.26) pero en el análisis de sensibilidad, ese incremento desaparece cuando se excluyen los estudios con sulfonilureas y glinidas y se toman en cuenta solamente las combinaciones de metformina con tiazolidinedionas, inhibidores DPP-4 e inhibidores SGLT2 (RR= 1.20; IC 95%= 0.91-1.56) 30.
La terapia combinada de metformina con sulfonilureas se asoció con el aumento estadística y clínicamente significativo del riesgo de hipoglicemia al compararla con monoterapia con metformina 31, y éste riesgo es mayor cuando la combinación incluyó glibenclamida (RR= 16.05; IC 95%= 6.22-41.39), que cuando se combinó con glimepiride (RR= 2.08; IC 95%= 0.74-5.86) o gliclazida (RR= 4.09; IC 95%= 2.13-7.89) 32.
Con relación a los cambios en el peso corporal, otro efecto que puede ser adverso o beneficioso en la terapia inicial, los estudios clínicos controlados demuestran que la combinación de metformina con tiazolidinedionas lo incrementan 33 mientras que la combinación de metformina con inhibidores SGLT2 lo reducen 34. En un meta-análisis de la combinación inicial de metformina con inhibidores DPP-4 se observó que ésta reduce la magnitud del descenso de peso de la metformina sola (Diferencia= 0.44, IC 95%= 0.22- 0.67) pero el efecto absoluto sigue siendo hacia la pérdida de peso 31.
Adicionalmente se tuvieron en cuenta otros efectos adversos potenciales como el riesgo de falla cardíaca, fracturas y cáncer de vejiga asociados con tiazolidinedionas 35-37 y el de infecciones del tracto urogenital asociado a inhibidores de SGLT2 38.
La evidencia presentada sugiere que el mejor balance de riesgo beneficio está a favor de la terapia combinada de metformina con un inhibidor de DPP-4, siendo opciones razonables la combinación de metformina con una sulfonilurea que tenga bajo riesgo de hipoglicemia (Glimepirida o glicazida), o la combinación de metformina con un inhibidor de SGLT-2.
Recomendaciones (Fig. 3)
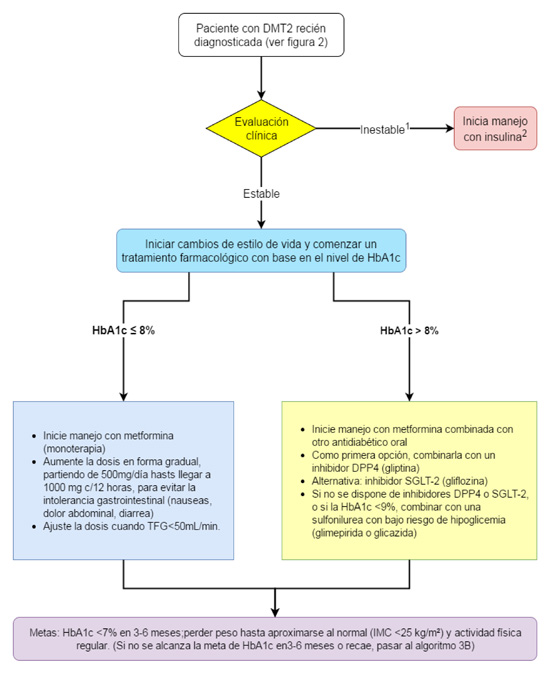
Figura 3.
Algoritmo para el manejo farmacológico inicial.
1 Paciente clínicamente inestable: muy sintomático, con pérdida aguda de peso, signos de deshidratación, evidencia de cetosis y glucemias muy elevadas,
2 Puede requerir insulina en combinación con otros antidiabéticos o en esquema intensivo. Su uso puede ser transitorio.
DMT2: diabetes mellitus tipo 2, HbA1c: hemoglobina glicosilada, TFG: tasa de filtración glomerular, DPP-4: dipeptidyl peptidasa 4, SGLT-2: co-transportador de sodio glucosa, IMC: Indice de masa corporal
9. En los pacientes con DMT2 recién diagnosticada y niveles de HbA1C >8%, se recomienda utilizar terapia combinada desde el inicio con metformina y otro antidiabético oral.
Recomendación fuerte a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
10. En los pacientes con DMT2 recién diagnosticada en quienes se decida implementar terapia combinada desde el inicio, se recomienda la asociación de metformina con un inhibidor de DPP-4.
Recomendación fuerte a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
11. En los pacientes con DMT2 recién diagnosticada en quienes se decida terapia combinada desde el inicio, se sugiere la combinación de metformina con un inhibidor SGLT-2, como una alternativa a la combinación de metformina con inhibidor DPP-4
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
12. En los pacientes con DMT2 recién diagnosticada y HbA1c >9% que no puedan utilizar la combinación de metformina con inhibidores de iDPP-4 o inhibidores de SGLT2, se sugiere la combinación de metformina con una sulfonilurea que tenga bajo riesgo de hipoglucemia (glimepirida o glicazida).
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
13. En los pacientes con DMT2 recién diagnosticada se sugiere no usar la combinación de metformina con glibenclamida, por el alto riesgo de hipoglucemia
Recomendación débil en contra. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
14. En los pacientes con DMT2 recién diagnosticada, se sugiere no usar la combinación de metformina con tiazolidinediona, por el riesgo aumentado de desarrollar edemas, falla cardiaca o fracturas.
Recomendación fuerte en contra. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
Puntos de buena práctica clínica
✔ Se deben preferir las combinaciones fijas de metformina con otro antidiabético oral siempre que estén disponibles porque mejoran la adherencia.
✔ La dosis de los inhibidores DPP-4 debe ajustarse cuando la tasa de filtración glomerular descienda por debajo de 50 mL/min, con excepción de linagliptina.
✔ Se recomienda en pacientes con DMT2 en quienes se decida el uso de sulfonilureas, hacer énfasis en la educación y realizar auto monitoreo de glucosa para detectar y tratar apropiadamente los episodios de hipoglucemia.
✔ No se recomienda usar sulfonilureas cuando la tasa de filtración glomerular descienda por debajo de 30 mL/min, con excepción de glipizida.
✔ Se recomienda vigilar y tratar oportunamente las infecciones genitourinarias cuando se usan los inhibidores SGLT2.
✔ La eficacia de los inhibidores de SGLT2 tiende a disminuir a medida que la función renal se deteriora significativamente y se debe consultar el inserto para suspenderlos en el momento oportuno.
✔ Si se presentan hipoglucemias con el uso de sulfonilureas, se debe considerar el cambio a medicamentos que no causen hipoglucemia.
Tema 3: Falla al tratamiento inicial
Premisas. El objetivo fundamental de la terapia farmacológica es lograr un adecuado control metabólico, manteniendo la HbA1c en la meta deseada sin causar efectos adversos y sin interferir negativamente en los cambios del estilo de vida
Si no se logra llevar la HbA1c a la meta en un lapso de 3 a 6 meses con el manejo inicial o si después de haberlo logrado ésta se eleva de nuevo, se debe intensificar el tratamiento y agregar otro antidiabético.
Pregunta clínica 5. ¿En pacientes con diabetes mellitus tipo 2 que ya iniciaron tratamiento farmacológico con metformina y no han alcanzado metas de control, cuál de los siguientes antidiabéticos se considera indicado como adición al tratamiento (segundo antidiabético), Sulfonilureas, Inhibidores DPP-4, tiazolidinedionas, agonistas del receptor de GPL1, inhibidores SGLT2, o Insulina basal?
Respuesta a la pregunta: En la revisión de la evidencia con respecto a la terapia de segunda línea en pacientes con DMT2 que no están controlados con dosis altas de metformina, se encuentra que las diferentes opciones terapéuticas (sulfonilureas, glinidas, tiazolidinedionas, inhibidores de DPP-4, inhibidores de SGLT-2, agonistas del receptor de GLP1, insulina basal, insulina bifásica) son efectivas al ser combinadas con metfomina 39-41. Cuando se comparan contra la adición de placebo, la HbA1c desciende entre 0.6 y 1% y hay 2 a 3 veces mayor probabilidad de alcanzar la meta de 7% o menos.
La diferencia entre dichas combinaciones radica principalmente en el perfil de eventos adversos y la seguridad en términos de hipoglicemia y patología cardiovascular entre otros.
La incidencia de hipoglicemia, importante marcador de seguridad, aumentó significativamente con la adición de sulfonilureas, glinidas o insulina, cosa que no ocurre con inhibidores de alfa-glucosidasas, DPP-4 o SGLT2 y tampoco con agonistas del receptor de GLP1 o tiazolidinedionas 39-41. Entre las diferentes sulfonilureas, la glibenclamida produce 4 a 8 veces más hipoglucemia que la glimepiridia o la gliclazida 31. El riesgo de hipoglucemia severa también se aumenta más de tres veces con sulfonilureas, especialmente cuando la HbA1c es menor y el IMC es mayor 42.
Con relación al peso corporal, éste se incrementó entre 1 y 3 kg al adicionar sulfonilureas, glinidas, tiazolidinedionas o insulina, siendo mayor el incremento con las tiazolidinedionas y la insulina bifásica 39-41. Los inhibidores de DPP-4 tienen en general un efecto neutro sobre el peso. Los inhibidores de SGLT2, pueden producir un descenso de peso de alrededor de 2 a 3 kg 38. La mayor reducción de peso se obtuvo con los agonistas del receptor de GLP1 que puede ser del orden de 1.4 a 3.7 kg 39-44.
Se tomó en consideración la evidencia ya mencionada en la pregunta anterior que sugiere un aumento del riesgo de falla cardiaca, riesgo de fracturas y de cáncer de vejiga asociado al uso de pioglitazona para la generación de la recomendación.
Recientemente se presentaron los estudios de seguridad cardiovascular a largo plazo con las nuevas clases de medicamentos. Ninguno de los tres estudios con inhibidores de DPP-4 mostró un aumento del riesgo de eventos cardiovasculares (Muerte cardiovascular, infarto no fatal, evento cerebrovascular no fatal, hospitalización por angina inestable) en un amplio espectro de pacientes con DMT2 (prevención primaria de alto riesgo, prevención secundaria, síndrome coronario agudo reciente) 45-47. Solo un estudio (con saxagliptina) mostró aumento de hospitalizaciones por falla cardíaca 47. No hubo aumento significativo de la incidencia de pancreatitis o de cáncer de páncreas, aunque los números fueron muy bajos.
Un estudio con un inhibidor de SGLT-2 tampoco demostró aumento del riesgo de infarto del miocardio y de eventos cerebrovasculares y por el contrario, se observaron reducciones muy tempranas y significativas de muerte cardiovascular (HR= 0.62; IC 95%= 0.49-0.77), muerte por cualquier causa (HR= 0.68; IC 95%= 0.57-0.82) y hospitalización por falla cardíaca (HR= 0.65; IC 95%= 0.50-0.85) 48.
Se llevó a cabo un análisis económico de costo-efectividad que apoya estas conclusiones 49. La combinación de metformina con sufonilureas, inhibidores de DPP-4 y pioglitazona es costo-efectiva. La combinación con un agonista del receptor de GLP-1 (exenatide) no es costo-efectiva. Cuando se hizo este análisis, no se incluyeron otros agonistas del receptor de GLP-1 y tampoco se incluyeron los inhibidores de SGLT-2 dado que la información con respecto a seguridad no estaba todavía disponible, pero los resultados preliminares de seguridad cardiovascular podrían justificar nuevas evaluaciones de costo-efectividad.
Teniendo en cuenta las opciones farmacológicas disponibles en nuestro medio, se consideró como primera elección en terapia de segunda línea la combinación de metfomina con un inhibidor de DPP-4 porque este grupo farmacológico contaba con el mejor perfil de efectividad y seguridad.
Como segunda opción se consideró el manejo con inhibidores de SGLT-2, aunque los estudios disponibles en la actualidad no aportan suficiente información para preferir esta terapia sobre los inhibidores de DPP-4 y al terminar esta guía, ninguno de los inhibidores de SGLT-2 había sido aprobado por el INVIMA.
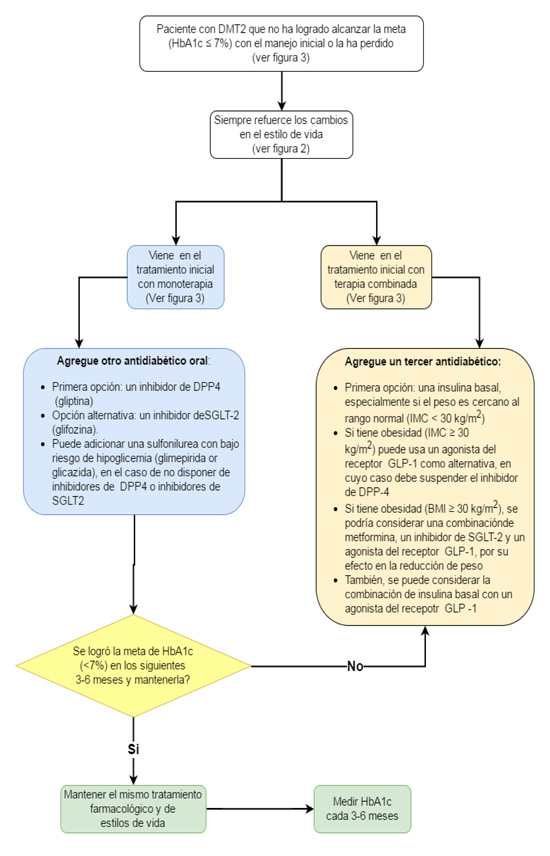
Recomendaciones (Fig. 4)
15. En los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia (HbA1C <7%), se recomienda adicionar un segundo antidiabético oral.
Recomendación fuerte a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
16. En los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia (HbA1C <7%), se recomienda, como primera opción, adicionar un inhibidor de DPP-4.
Recomendación fuerte a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
17. En los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia (HbA1C <7%), se sugiere adicionar inhibidor de SGLT2 como alternativa al inhibidor de DPP-4.
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
18. En los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia (HbA1C <7%), se sugiere agregar una sulfonilureas que tenga bajo riesgo de hipoglucemia (glimepirida, glicazida) cuando no se hallen disponibles o estén contraindicados los inhibidores de DPP-4 o de SGLT2.
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
19. Se sugiere no adicionar glibenclamida al manejo de los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia, por el alto riesgo de hipoglucemia.
Recomendación débil en contra. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
20. Se sugiere no adicionar tiazolidinedionas al manejo de los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia, por el mayor riesgo de edema, falla cardiaca y fracturas con esta terapia.
Recomendación débil en contra. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
21. En los pacientes con DMT2 que no han alcanzado la meta terapéutica o la han perdido con metformina como monoterapia (HbA1C <7%) y que persisten obesos (IMC= ≥30 kg/m²), se sugiere la adición de un agonista del receptor de GLP-1 por el potencial beneficio sobre la reducción de peso.
Recomendación fuerte a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
Puntos de buena práctica clínica
✔ Siempre que se detecte una falla en el logro o el mantenimiento de las metas terapéuticas con los fármacos, se deben revisar e intensificar también los cambios del estilo de vida.
✔ La intensificación de los cambios en el estilo de vida debe incluir una pérdida significativa de peso. Al respecto, se debe tener en cuenta que las sulfonilureas y las tiazolidinedionas lo incrementan, los inhibidores de DPP-4 no lo modifican, la metformina puede bajarlo y los inhibidores de SGLT2 lo reducen al igual que los agonistas del receptor de GLP1.
✔ Se debe brindar educación desde el inicio a los pacientes que requieran sulfonilureas con el fin de prevenir, detectar y tratar oportunamente los episodios de hipoglucemia.
✔ Si se presentan hipoglucemias con la adición de sulfonilureas, se debe considerar el cambio a medicamentos que no causen hipoglucemia.
✔ La adición de un agonista del receptor de GLP-1 requiere educar al paciente en el uso de la inyección subcutánea y la titulación de la dosis que debe incrementarse gradualmente para minimizar los efectos gastrointestinales como la náusea y el vómito.
✔ Cuando el paciente se encuentra muy sintomático y clínicamente inestable, con pérdida aguda de peso, signos de deshidratación, evidencia de cetosis y glucemias muy elevadas, se recomienda agregar insulina
Pregunta clínica 6. ¿En pacientes con diabetes mellitus tipo 2 que ya iniciaron tratamiento farmacológico con metformina y un segundo medicamento antidiabético y no han alcanzado metas de control, cuál antidiabético se considera indicado como adición al tratamiento (tercer antidiabético)?.
Respuesta a la pregunta. Una revisión sistemática 50 evaluó el efecto de la adición de un tercer medicamento, sumado a glibenclamida y metformina, sobre los niveles de HbA1c, peso corporal y presencia de episodios de hipoglicemia.
La asociación de tiazolidinedionas al tratamiento con glibenclamida y metformina fue la combinación que mayor disminución produjo en la HbA1c (-1.15%; IC 95%= -1.35--0.95%) al compararla con placebo, seguida de los agonistas del receptor de GLP-1 (-1.04%; IC 95%= -1.24--0.85%), los inhibidores de DPP-4 (-0.89%; IC 95%= -1.11--0.67%) y la insulina (-0.77%; IC 95%= -0.95--0.47%), siendo todos los resultados estadísticamente significativos.
Al comparar con insulina en combinación con metformina y glibenclamida, las tiazolidinedionas producen una mayor reducción de la HbA1c que es estadísticamente pero no clínicamente significativa (0.22%; IC 95%= 0.07-0.31%). Los agonistas del receptor de GLP-1 en comparación con insulina no demostraron una diferencia significativa.
En cuanto al cambio en el peso corporal, los agonistas de GLP-1 tienden a reducirlo y las tiazolidinedionas a aumentarlo, pero sin alcanzar la significancia estadística. La combinación con insulina si aumentó el peso de una manera estadísticamente y clínicamente significativa (2.31 Kg; IC 95%= 0.13-4.48 Kg). Para los inhibidores DPP-4 solo se cuenta con información de un estudio en el cual no se tuvo en cuenta el peso corporal de los pacientes.
Se revisó también un meta-análisis en red entre los diferentes medicamentos como tercer anti diabético 42. Allí se encontró que ninguno de los medicamentos analizados (agonistas del receptor de GLP-1, tiazolidinedionas, inhibidores de DPP-4 e insulina) generó una disminución estadísticamente significativa de los niveles de HbA1c al ser comparados entre sí. Con relación al peso corporal, solamente los agonistas del receptor de GLP-1 lo redujeron significativamente (-1.63 Kg; IC 95%= -2.71;-0.60), mientras que los otros medicamentos no mostraron cambios significativos.
La información en cuanto a episodios de hipoglicemia severa es muy limitada, sin poder generar datos con significancia estadística.
La comparación de desenlaces críticos como mortalidad, complicaciones microvasculares (nefropatía, retinopatía, neuropatía), complicaciones macrovasculares (ACV, IAM, Enfermedad arterial periférica), abandono (adherencia) y calidad de vida (el desenlace calificado como importante) se incluyó en el objetivo de un meta análisis 51 pero los datos no eran consistentes en todos los ensayos clínicos y los periodos de seguimiento fueron relativamente cortos, por lo que no fue posible hacer un análisis y obtener conclusiones al respecto. Otro meta-análisis evaluó el riesgo de eventos cardiovasculares mayores al comparar los agonistas del receptor de GLP-1 con otros antidiabéticos 52 y no encontró diferencias estadísticamente significativas.
Recomendaciones (Fig. 4)
22. Se sugiere como tercera medicación antidiabética agregar insulina basal a los pacientes que con la combinación de dos fármacos no logran alcanzar la meta de HbA1c o la han perdido y no están obesos (IMC= <30 kg/m²).
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
23. Se sugiere la adición de agonista del receptor de GLP-1 como tercera medicación antidiabética a los pacientes que con la terapia oral combinada no logran alcanzar la meta de HbA1c o la han perdido y persisten obesos (IMC ≥30 kg/m²).
Recomendación débil a favor. Calidad de la evidencia Moderada ⴲ ⴲ ⴲ ⴱ
24. Se sugiere considerar la asociación de metformina, inhibidores de SGLT-2 y agonista del receptor de GLP-1 únicamente en los pacientes que no logran alcanzar la meta de HbA1c o la han perdido con terapia dual y que persistan obesos (IMC ≥30).
Recomendación débil a favor. Consenso de expertos
Puntos de buena práctica clínica
✔ La insulina NPH se puede utilizar como insulina basal cuando se inyecta a la hora de acostarse, hacia las 10-11 pm.
✔ Las insulinas análogas de acción prolongada (glargina U100 y U300, detemir, degludec) tienen menor riesgo de hipoglucemia cuando se comparan con la insulina NPH, por lo cual se prefieren cuando se desea que el paciente se mantenga en un control óptimo evitando hipoglucemias, o cuando estas se presentan al intentar alcanzar la meta de control glucémico. Estas insulinas se inyectan una vez al día a una hora fija, excepto el detemir que puede administrarse dos veces al día si es necesario.
✔ La dosis inicial de insulina basal es de 10 unidades/día o de 0.2 unidades/kg de peso/día. Existen varios algoritmos para titularla, y todos se basan en incrementar la dosis en 2 a 4 unidades cada vez que la glucemia en ayunas está por encima del valor prefijado por dos a tres días seguidos o en el promedio de ese mismo intervalo.
✔ Los agonistas del receptor de GLP-1 requieren una titulación progresiva para minimizar los efectos secundarios gastrointestinales y cada uno tiene sus instrucciones al respecto. Así mismo cada uno tiene su propia forma de administración que puede ser una o dos veces al día o inclusive semanal.
✔ Cuando no se logra la respuesta esperada con la insulina basal o con los agonistas del receptor GLP-1, se pueden combinar o se pueden utilizar esquemas de insulinoterapia intensiva. Sin embargo en estos casos se recomienda que un equipo especializado reevalúe la meta y la necesidad de intensificar el tratamiento en cada paciente.
✔ Durante la terapia con insulina en combinación con antidiabéticos orales que puedan causar hipoglucemia, se debe educar al paciente en la detección temprana de los síntomas de hipoglucemia, así como en las acciones correctivas en caso de que se presente. Se debe poner especial cuidado en este sentido al combinar insulina con tratamientos que incluyan sulfonilureas. Si se presentan hipoglucemias y la insulina sigue siendo necesaria, se debe cambiar la sulfonilurea por otro medicamento que no cause hipoglucemia.
Tema 4. Metas del control glucemico
Premisas. Alcanzar y mantener una HbA1c promedio de 7% reduce la incidencia de complicaciones micro y macrovasculares de la DMT2.
El límite superior normal analítico de la HbA1c está alrededor de 6% pero los estudios clínicos controlados no han mostrado que la intensificación del tratamiento para alcanzar una HbA1c normal (<6.5%) produzca beneficios que superen los riesgos en la mayoría de los pacientes con DMT2.
El control metabólico de los pacientes con DMT2 debe estar dirigido a alcanzar y mantener una meta de HbA1c ≤7% sin que esto produzca riesgos que superen los beneficios y evitando hasta donde sea posible los efectos adversos y el deterioro de la calidad de vida.
En pacientes con DMT2 sin comorbilidades serias y con edad ≤65 años se puede disminuir los niveles de HbA1c hasta 6.5%, especialmente si ya tienen indicios de microangiopatía. Lo anterior siempre y cuando no produzca riesgos que superen los beneficios y evitando hasta donde sea posible los efectos adversos y el deterioro de la calidad de vida.
Pregunta clínica 7. ¿En personas adultas mayores de 65 años con diabetes mellitus tipo 2 se requiere una individualización de la meta de control glucémico diferente a la meta de hemoglobina glicosilada igual o menor a 7%?
Respuesta a la pregunta. La evidencia evaluada demuestra que:
• El tratamiento intensificado enfocado a obtener como meta de manejo una HbA1c cercana al valor normal no impacta el riesgo de mortalidad global, ni el riesgo de mortalidad de origen cardiovascular, tanto en la población general como en el subgrupo de mayores de 60 años, aunque se observó heterogeneidad en este último grupo (RR= 1.13; IC 95%= 0.81-1.57, I²= 72%) 53.
• En un estudio para evaluar el beneficio del control glucémico intensivo (HbA1c <6%) sobre el riesgo cardiovascular que tuvo que ser suspendido por un aumento de la mortalidad en el grupo de control intensivo, el análisis de subgrupos demostró que dicho aumento fue significativo en menores de 65 años pero no en los que tenían mayor edad (HR= 0.97; IC 95%= 0.7-1.36 para mortalidad cardiovascular y HR= 1.06 IC 95%= 0.84-1.34 para muerte por cualquier causa). Por el contrario, la disminución en la incidencia de infarto del miocardio no fatal se observó solo en el subgrupo de menores de 65 años en ese mismo análisis. La incidencia de hipoglucemia que requirió asistencia médica fue casi el doble en los que tenían 65 o más años (incidencia anual 4.45% vs. 2.45%) y de hecho la hipoglucemia fue tan frecuente al inicio del estudio en mayores de 80 años que la inclusión de pacientes en este grupo etáreo se suspendió 54.
• El tratamiento enfocado a obtener como meta una HbA1c cercana al valor normal no impacta el riesgo de ataque cerebrovascular en la población general de personas con DMT2. Hallazgos similares se encontraron en el subanálisis teniendo en cuenta exclusivamente mayores de 62 años (RR= 1.01; IC 95%= 0.91-1.11) 55.
• No existen datos específicos a calidad de vida para mayores de 65 años, sin embargo los obtenidos en la población general sugieren que no hay impacto del manejo intensificado en las mediciones de estado general de salud, síntomas asociados a la diabetes o depresión.
• Una revisión sistemática reciente con una muestra grande (34,912 pacientes DMT2 con edades hasta 72 años) no logró hacer el análisis planeado para el grupo ≥65 años pero encontró que en general el control glucémico intensivo reduce significativamente la incidencia de infarto del miocardio no fatal (RR= 0.87; IC 95%= 0.77-0.98) y de amputaciones (RR= 0.45; IC 95%= 0.45-0.94) con calidad moderada de la evidencia y aumenta el riesgo de hipoglucemia (RR= 2.18; IC 95%= 1.53-3.11) con calidad alta de la evidencia. No parece tener efecto sobre la incidencia de mortalidad, evento cerebrovascular no fatal o enfermedad renal terminal 56.
• Teniendo en cuenta esta información, el grupo desarrollador de la guía consideró que no existe un beneficio significativo en dar un tratamiento intensificado enfocado a obtener como meta de manejo HbA1c cercana al valor normal en pacientes mayores de 65 años, y que por el contrario este grupo de pacientes tiene un riesgo más alto de hipoglicemia, por lo que se decidió no recomendarlo.
Así mismo el grupo desarrollador de la guía concluyó que no existe evidencia alguna que demuestre que buscar una meta de manejo más alta mejore en balance riesgo-beneficio, por lo que en pacientes mayores de 65 años, sin otras comorbilidades y funcionalmente independientes se deberá buscar una meta de manejo igual a la utilizada para pacientes de menor edad, es decir HbA1c ≤7%, tratando de minimizar el riesgo de hipoglucemia.
Deberán tenerse en cuenta subgrupos de pacientes mayores de 65 años, donde los riesgos de hipoglicemia son más altos, y que por tanto requieren ajustar las metas de manejo. Si bien no existen experimentos clínicos que cuantifiquen ese riesgo, se decidió individualizar los pacientes con fragilidad, demencia o depresión, así como aquellos pacientes en cuidados de fin de vida. Para este enfoque se decidió tener en cuenta GPC desarrolladas por otros grupos, que generaron las recomendaciones de manejo para estos pacientes basados en consenso de expertos 57-59. La decisión del grupo desarrollador de la guía fue pues sugerir metas de manejo con un máximo de HbA1c de 8%, en pacientes funcionalmente dependientes, incluyendo aquellos con fragilidad o demencia, según las definiciones sugeridas por la Federación Internacional de Diabetes 58.
Recomendaciones
25. En los pacientes con DMT2 mayores de 65 años, se recomienda no intensificar el manejo para alcanzar valores de HbA1c cercanos a lo normal (<6.5% HbA1c).
Recomendación fuerte en contra. Calidad de la evidencia alta ⴲ ⴲ ⴲ ⴲ
26. En los pacientes con DMT2 mayores de 65 años funcionalmente independientes y libres de otras comorbilidades mayores, se recomienda dar manejo dirigido a alcanzar los mismos niveles de HbA1c recomendados para la población menor de 65 años (≤7%)
Recomendación fuerte a favor. Calidad de la evidencia alta ⴲ ⴲ ⴲ ⴲ
27. En los pacientes con DMT2 mayores de 65 años que presenten fragilidad* o demencia**, o en quienes se anticipe riesgo aumentado de hipoglucemia***, se sugiere un manejo menos intensivo con valores de HbA1c entre 7% y 8%.
Recomendación débil a favor. Consenso de expertos
* Pacientes con fatiga significativa, restricción severa en movilidad y fuerza, con riesgo incrementado de caídas y de institucionalización.
** Pacientes con déficit cognitivo que condiciona problemas significativos de memoria, desorientación, cambios de personalidad, o que tengan dificultades para autocuidado.
*** Pacientes en tratamiento con drogas que causan hipoglucemia (sulfonilureas, metiglinidas o insulina) y tienen otros factores que puedan incrementar este riesgo (depresión, pobre soporte social, inapetencia o intolerancia a la ingesta).
28 En los pacientes con DMT2 que se encuentren en cuidados de fin de vida+, se sugiere limitar el objetivo del tratamiento a evitar la hiperglucemia sintomática.
Recomendación débil a favor. Consenso de expertos
+ Pacientes que cumplan con los criterios de enfermo en fase terminal definidos en la ley 1733 de 2014 o la resolución 1216 de 2015 (Referente a derecho a morir con dignidad). Se define enfermo en fase terminal a todo aquel que es portador de una enfermedad o condición patológica grave, que haya sido diagnosticada en forma precisa por un médico experto, que demuestre un carácter progresivo e irreversible, con pronóstico fatal próximo o en plazo relativamente breve, que no sea susceptible de un tratamiento curativo y de eficacia comprobada, que permita modificar el pronóstico de muerte próxima; o cuando los recursos terapéuticos utilizados con fines curativos han dejado de ser eficaces.
Puntos de buena práctica clínica
✔ Considerando que la población mayor de 65 años es muy heterogénea, es necesario realizar una valoración funcional integral del paciente para establecer los objetivos terapéuticos.
Pregunta clínica 8. ¿En personas adultas con diabetes mellitus tipo 2 y enfermedad cardiovascular, se requiere una individualización de la meta de control glucémico diferente a la meta de hemoglobina glicosilada igual o menor de 7%?
Respuesta a la pregunta. Se identificaron varias revisiones sistemáticas que compararon el manejo intensivo con hipoglucemiantes y/o insulina con el fin de llegar a metas de HbA1c cercanas al valor normal vs esquemas de manejo convencional con metas menos estrictas, 53, 60, en las cuales se incluyeron y analizaron de forma independiente los pacientes con antecedente de enfermedad coronaria. Una revisión sistemática 53 documentó que cuando se comparó el manejo intensivo vs el convencional en pacientes con antecedente de enfermedad cardiovascular vs aquellos que no la tenían no hubo un cambio con respecto al riesgo de morir por una causa cardiovascular, con un RR= 1.13 (IC 95%= 0.81-1.57) vs sin antecedente RR= 0.89 (IC 95%= 0.74-1.08).
Al analizar de forma independiente el estudio ACCORD 60 donde aproximadamente un tercio de los sujetos con DMT2 tenían antecedente de enfermedad cardiovascular establecida, se encontró que el manejo intensivo comparado con el convencional no generó un cambio en el riesgo de sufrir el desenlace primario, y por el contrario el estudio fue terminado de forma temprana al observar una mayor mortalidad en el grupo de manejo intensivo que en el grupo convencional. En el análisis pre-establecido de subgrupos no se encontró una diferencia en la incidencia de mortalidad entre los que tenían y los que no tenían una enfermedad cardiovascular previa, aunque estos últimos tuvieron una incidencia significativamente menor del desenlace compuesto primario (Definido como infarto, ataque cerebrovascular o muerte de origen cardiovascular).
Esto se demostró también en una revisión sistemática de cuatro estudios que incluyó el anterior 61, donde el análisis exploratorio de subgrupos mostró que al comparar la terapia intensiva con la convencional, parecía haber un efecto diferencial sobre desenlaces cardiovasculares mayores en pacientes con y sin antecedentes de enfermedad macrovascular, siendo significativamente favorable para los últimos y no significativa para los primeros (HR= 1.00; IC 95%= 0.89-1.13, vs HR= 0.84, IC 95%= 0.74-0.94, respectivamente; p= 0.04 para interacción). Por el contrario, en otro meta-análisis los autores no encontraron interacción del antecedente de enfermedad isquémica del corazón con el efecto del control glucémico intensivo sobre eventos cardiovasculares incluyendo los fatales 62.
De acuerdo a la evidencia presentada se consideró que la intensificación del manejo para llegar a metas de HbA1c cercanas al valor normal en pacientes con antecedente de enfermedad cardiovascular no mostró una reducción en el riesgo de morir, ni de los desenlaces de origen cardiovascular incluyendo eventos cardiovasculares mayores. Igualmente se consideró que no había justificación para recomendar una meta superior en los pacientes con antecedente de enfermedad cardiovascular.
Recomendaciones
29. En los pacientes con DMT2 y con antecedente de enfermedad cardiovascular la meta de hemoglobina glicosilada no debe ser diferente a la meta general (igual o menor a 7%) y no se recomienda la intensificación del tratamiento para alcanzar un valor de HbA1c cercano al normal (HbA1c <6.5%).
Recomendación fuerte en contra. Calidad de la evidencia moderada ⴲ ⴲ ⴲ ⴱ
Tema 5: Detección de complicaciones
Premisas. Las personas con DMT2 tienen un riesgo 2 a 4 veces mayor de sufrir un evento coronario en comparación con las personas sin diabetes, y en algunos estudios epidemiológicos se ha demostrado que este riesgo es equivalente al de personas sin diabetes con enfermedad coronaria.
Por ser un equivalente coronario, las personas que tienen DMT2 deben controlar los factores de riesgo cardiovasculares, aplicando el mismo manejo estricto que se recomienda en la prevención secundaria de la enfermedad coronaria para el control de los lípidos y la presión arterial. Al aplicar este manejo se cuestiona la tamización de la enfermedad coronaria mientras no sea sintomática. Las pruebas de tamización para la enfermedad coronaria incluyen la prueba de esfuerzo convencional, pruebas de estrés farmacológico con ecocardiografía o con imágenes de perfusión por medicina nuclear y la cuantificación del puntaje de calcio coronario por tomografía computarizada. El electrocardiograma suele hacerse de rutina en personas mayores de 40 años pero no se considera una prueba adecuada para la tamización de la enfermedad coronaria por su baja sensibilidad y especificidad.
El daño vascular producido por la hiperglucemia sostenida en el paciente con DMT2 también se manifiesta en los capilares como micro angiopatía. Las principales manifestaciones clínicas se ven en la retina (retinopatía), el glomérulo (nefropatía) y los nervios periféricos (neuropatía).
Como la DMT2 suele comenzar en forma silenciosa, puede transcurrir un tiempo largo desde el inicio de la enfermedad hasta el diagnóstico y no es infrecuente encontrar manifestaciones clínicas de micro angiopatía en el paciente con DMT2 recién diagnosticada. Esto obliga a la búsqueda sistemática (tamización) de estas complicaciones desde el inicio, y luego anualmente con el fin intensificar el control para evitar su progresión. La tamización de retinopatía se hace mediante la fotografía no midriática de la retina o por oftalmoscopia hecha por un profesional especializado. La tamización de nefropatía se hace midiendo la presencia de albúmina en la orina y estimando la tasa de filtración glomerular. La tamización de neuropatía se hace evaluando la sensibilidad vibratoria y táctil en tobillos y pies.
Pregunta clínica 9. ¿En personas adultas con diabetes mellitus tipo 2 y sin síntomas de insuficiencia coronaria se debe hacer tamización para enfermedad arterial coronaria?
Respuesta a la pregunta. En la revisión de la mejor evidencia disponible se encontraron tres estudios clínicos 63-65, de cuya evaluación se concluye que la realización de pruebas de tamización para enfermedad coronaria silente en pacientes con diabetes tipo 2 asintomáticos con y sin factores de riesgo cardiovasculares no reduce la incidencia de eventos cardiovasculares: no tiene impacto sobre infarto agudo de miocardio no fatal (RR= 0.61; IC 95%= 0.29-1.29), ni tampoco sobre muerte por cualquier causa (RR= 1.18; IC 95%= 0.72-1.93). Tampoco demostró tener impacto estadística ni clínicamente significativo sobre la frecuencia de revascularizaciones que fue similar en los estudios clínicos controlados.
Por último vale la pena mencionar que la realización de estas pruebas en pacientes diabéticos tipos 2 asintomáticos conlleva a procedimientos innecesarios y costosos, que al final terminan haciéndose en los pacientes no tamizados cuando presentan síntomas, sin que la enfermedad tenga un curso diferente.
Recomendaciones
30. En los pacientes con DMT2 sin síntomas de insuficiencia coronaria, se sugiere no hacer tamización para enfermedad arterial coronaria.
Recomendación débil en contra. Calidad de la evidencia baja ⴲ ⴱⴱⴱ
Puntos de buena práctica clínica
✔ En todo paciente con DMT2 se deben manejar los factores de riesgo cardiovascular como si se tratara de una persona con enfermedad coronaria establecida. La única con excepción radica en la administración de aspirina a bajas dosis, que todavía no se recomienda en todas las personas con DMT2 sin enfermedad cardiovascular establecida.
✔ El proceso de diagnóstico de la enfermedad coronaria se debe iniciar cuando el paciente presente síntomas sugestivos de enfermedad coronaria, y según los hallazgos se procederá al tratamiento oportuno y apropiado.
✔ La persona con DMT2 debe conocer cuáles son los síntomas clásicos de isquemia coronaria y los no clásicos como disnea de aparición repentina, para que los pueda identificar oportunamente.
Pregunta clínica 10. ¿En personas adultas con DMT2 cómo debe hacerse el manejo según los resultados de la tamización para albuminuria?
Respuesta a la pregunta. Una revisión sistemática de la optimización de la tamización para enfermedad renal en diabetes y el impacto del tratamiento 66 demostró para el caso de DMT2 que la excreción urinaria de albúmina se redujo en un 21% (IC 95%= 7-32%) en aquellos que tenían normoalbuminuria y en un 27% (IC 95%= 15-38%) en aquellos que tenían microalbuminuria después de un tratamiento con inhibidores de la enzima convertidora de angiotensina (IECA) o antagonistas del receptor de angiotensina (ARA II) cuando se compararon con los que no recibieron ese tratamiento, aunque la respuesta fue muy heterogénea (I2= 85% y 87% respectivamente). Tanto los pacientes con normoalbuminuria como los que tenían microalbuminuria se beneficiaron con estos tratamientos en términos de progresión y regresión. El riesgo relativo de progresión de normo a microalbuminuria fue de 0.84 (IC 95%= 0.79-0.89) y de micro a macroalbuminuria fue de 0.52 (IC 95%= 0.43-0.63). Así mismo, un mayor número de pacientes regresó de micro a normoalbuminuria en el grupo tratado (RR= 1.2; IC 95%= 1.12-1.29) aunque la heterogeneidad fue alta (I2= 75%). No hubo efecto significativo sobre la filtración glomerular o sobre mortalidad aunque el tiempo de seguimiento fue muy corto para evaluar este tipo de desenlace. No se encontró diferencia en la respuesta al hacer un análisis de sensibilidad entre el uso de comparador antihipertensivo y no-antihipertensivo (p= 0.86).
En pacientes con DMT2 normotensos, el tratamiento con ARA II también redujo la excresión urinaria de albúmina (Relación de medias= 0.57; IC 95%= 0.47- 0.69) 67. Un efecto similar se puede esperar con el uso de IECA 68.
Sin embargo la evidencia del tratamiento de microalbuminuria en el paciente normotenso con DMT2 no ha sido suficiente para demostrar un efecto sobre eventos cardiovasculares o desenlaces relacionados con la función renal 69-71. Adicionalmente se debe tener en cuenta que en la reunión de la Food and Drug Administration (FDA) y la National Kidney Foundation realizada en 2008, se concluyó que la evidencia disponible es insuficiente para determinar que el uso de los niveles de albuminuria pueda ser empleado como una medida de desenlace clínico en pacientes con diabetes.
No se encontró evidencia en los documentos previamente presentados respecto a los siguientes desenlaces: enfermedad cardiovascular, paso a nefropatía estadio III o necesidad de diálisis.
Recomendaciones (Fig. 5)
Figura 5.
Algoritmo para la tamización de albuminuria.
DMT2: diabetes mellitus tipo 2, IECA: inhibidor de la enzima convertidora de angiotensina, ARA-2: antagonista del receptor de angiotensina 2
31. En los pacientes con DMT2, se sugiere iniciar tratamiento con un inhibidor de la enzima convertidora de angiotensina (IECA) o un antagonista del receptor de angiotensina 2 (ARA2) cuando se detecte microalbuminuria persistente*, y aunque todavía no tengan hipertensión arterial.
Recomendación débil a favor de la intervención. Calidad de la evidencia moderada ⴲ ⴱⴱⴱ.
32. Se sugiere no dar tratamiento con IECA o ARA2 en pacientes con DMT2 que no presenten hipertensión arterial ni microalbuminuria *.
Recomendación débil en contra de la intervención. Calidad de la evidencia moderada ⴲ ⴱⴱⴱ
*Proporción ≥30 mg de albuminuria/g de creatinuria en una muestra aislada de la primera orina de la mañana o ≥30 mg de albumina en la orina recolectada durante 24 horas, que persista en una segunda muestra tomada con un intervalo de 4 a 6 semanas.
Puntos de buena práctica clínica
✔ Para evaluar la presencia de microalbuminuria se prefiere medir la albuminuria y la creatinuria en una muestra de la primera orina de la mañana y calcular la proporción microalbuminuria (mg)/creatinuria (g).
✔ La prueba de tamización para microalbuminuria se debe hacer anualmente desde el momento del diagnóstico de DMT2. Debido a que existen múltiples factores que pueden aumentar la excreción de albumina de manera transitoria, se debe confirmar su persistencia en al menos 2 de 3 mediciones, en muestras tomadas con intervalos de 4 a 6 semanas.
✔ La nefropatía diabética se diagnostica cuando, además de la presencia de microalbuminuria, la tasa de filtración glomerular estimada (TFGe) está por debajo de 60 mL/min. La TFGe se calcula utilizando fórmulas como MDRD, Cockroft o CKD-Epi que tienen en cuenta la creatinina sérica, la edad y en algunas el peso. Además se ajustan por sexo femenino y por raza negra. La última es la más utilizada actualmente.
✔ En el paciente con DMT2, el control estricto de la hipertensión arterial previene y reduce la progresión de la nefropatía diabética. Se comienza el manejo con IECA o ARA2 pero se deben agregar otros antihipertensivos si es necesario para lograr una meta de presión arterial sistólica (PAS) entre 130 y 139 mmHg y de presión arterial diastólica (PAD) ≤80 mmHg.
✔ Cuando la albuminuria es >300 mg/g de creatinina (>300 mg en 24 horas) se clasifica como macroalbuminuria y se considera equivalente a la presencia de proteinuria. Su persistencia indica un mayor riesgo de mortalidad y de progresión a estadios avanzados de falla renal por lo cual requiere un manejo aún más estricto.
Indicadores de seguimiento de la implementación de la GPC
Los indicadores propuestos pretenden apoyar el proceso de implementación, evaluar la adherencia a las recomendaciones y valorar el impacto de la GPC. En la medida en que la información obtenida sea oportuna, confiable y precisa, estos podrán utilizarse como insumo para retroalimentar el proceso de implementación y favorecer el desarrollo de las GPC (Tabla 3). El proceso completo de desarrollo de estos indicadores puede consultarse en la versión completa de la guía disponible en la página web del Ministerio de Salud y Protección Social (http://gpc.minsalud.gov.co/guias/Documents/diabetes/DIABETES_TIPO_2_COMPLETA.pdf).
| Tipo de indicador | Nombre del indicador | Operacionalización | Periodicidad | Fuente primaria | Meta |
|---|---|---|---|---|---|
| Estructura | Porcentaje de laboratorios que hacen la medición de la HbA1c de acuerdo con los métodos recomendados por el NGSPP (www.ngsp.org). | Número de laboratorios que hacen la medición de la HbA1c de acuerdo con los métodos recomendados por NGSPP / Número de laboratorios que hacen la medición de HbA1c x 100. | Anual | EPS | Primer año: 50%. Tercer año: 100%. |
| Proceso | Porcentaje de pacientes con DMT2 (Código CIE-10: E11) en quienes se hacen al menos dos mediciones de HbA1c al año. | (Número de pacientes con diagnóstico clínico de Diabetes tipo 2 (Código CIE-10: E11) en quienes se hacen dos o más mediciones de HbA1c durante el año / Número total de pacientes con diagnóstico clínico de DMT2 (Códigos CIE-10 E11)*100 | Anual | IPS | Primer año: 60%. Tercer año: 90% |
| Porcentaje de pacientes con Diabetes tipo 2 (Código CIE-10: E11) en quienes se realiza una medición anual de microalbuminuria | Número de pacientes con diagnóstico clínico de DMT2 (Código CIE-10: E11) en quienes se hace una medición de microalbuminuria durante el año / Número total de pacientes con diagnóstico clínico de DMT2 (Códigos CIE-10 E11)*100. | Anual | IPS | Primer año: 50%. Tercer año: 90% | |
| Resultado | Porcentaje de pacientes con Diabetes tipo 2 (Código CIE-10: E11) con niveles de hemoglobina glucosilada (HbA1c) iguales o menores al 7% | Número de pacientes con diagnóstico clínico de DMT2 (Código CIE-10: E11) con valores HbA1c ≤7%/ Número total de pacientes con diagnóstico clínico de DMT2 (Códigos CIE-10 E11)*100. | Semestral | IPS | primer año: 40%. tercer año: 70%. |
Referencias
Aschner P. Epidemiología de la diabetes en Colombia. Avances Diabetol. 2010;26:95–100 | |
Federación Internacional de diabetes. ATLAS de la DIABETES de la FID. 6th. Bruselas, Bélgica: Federación Internacional de Diabetes; 2014 | |
Aschner PJ, Ruiz AJ. Metabolic memory for vascular disease in diabetes. Diabetes Technol Ther. 2012;14 1:S68–S74 | |
United Kingdom Prospective Diabetes Study. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33). Lancet. 1998;352(9131):837–853 | |
Holman RR, Paul SK, Bethel MA, Matthews DR, Neil HAW. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med. 2008;359(15):1577–1589 | |
Gaede P, Vedel P, Larsen N, Jensen GVH, Parving H-H, Pedersen O. Multifactorial intervention and cardiovascular disease in patients with type 2 diabetes. N Engl J Med. 2003;348(5):383–393 | |
Gaede P, Lund-Andersen H, Parving H-H, Pedersen O. Effect of a multifactorial intervention on mortality in type 2 diabetes. N Engl J Med. 2008;358(6):580–591 | |
Tankova T, Chakarova N, Atanassova I, Dakovska L. Evaluation of the Finnish Diabetes Risk Score as a screening tool for impaired fasting glucose, impaired glucose tolerance and undetected diabetes. Diabetes Res Clin Pract. 2014;92(1):46–52 | |
Asociación latinoamericana de diabetes. Guias ALAD 2013 para el Diagnostico y Manejo de la Diabetes Mellitus tipo 2 con Medicina basada en Evidencia. Edicion 2013. Rev ALAD. 2013;1–142 | |
Balshem H, Helfand M, Schünemann HJ, Oxman AD, Kunz R, Brozek J, et al. GRADE guidelines: 3. Rating the quality of evidence. J Clin Epidemiol. 2011;64(4):401–406 | |
Simmons RK, Rahman M, Jakes RW, Yuyun MF, Niggebrugge AR, Hennings SH, et al. Effect of population screening for type 2 diabetes on mortality: Long-term follow-up of the Ely cohort. Diabetologia. 2011;54(2):312–319 | |
Lindström T, Tuomilehto J. The Diabetes Risk Score. A practical tool to predict type 2 diabetes risk. Diabetes Care. 2003;26(3):725–731 | |
Makrilakis K, Liatis S, Grammatikou S, Perrea D, Stathi C, Tsiligros P, et al. Validation of the Finnish diabetes risk score (FINDRISC) questionnaire for screening for undiagnosed type 2 diabetes, dysglycaemia and the metabolic syndrome in Greece. Diabetes Metab. 2011;37(2):144–151 | |
Soriguer F, Valdés S, Tapia MJ, Esteva I, Ruiz de Adana MS, Almaraz MC, et al. Validación del FINDRISC (FINnish Diabetes Risk SCore) para la predicción del riesgo de diabetes tipo 2 en una población del sur de España. Estudio Pizarra. Med Clin (Barc). 2012;138(9):371–376 | |
Schwarz P, Li J, Lindstrom J, Tuomilehto J. Tools for predicting the risk of type 2 diabetes in daily practice. Horm Metab Res. 2009;41(2):86–97 | |
Aschner P, Buendía R, Brajkovich I, Gonzalez A, Figueredo R, Juarez XE, et al. Determination of the cutoff point for waist circumference that establishes the presence of abdominal obesity in Latin American men and women. Diabetes Res Clin Pract. 2011;93(2):243–247 | |
Aschner P, Nieto R, Marin A, Rios M. Evaluation of the FINDRISK score as a screening tool for people with impaired glucose regulation in Latin America using modified score points for waist circumference according to the validated cutoff values for abdominal obesity. Minerva Endocrinol. 2012;37:114–118 | |
Simmons RK, Echouffo-Tcheugui JB, Sharp SJ, Sargeant AL, Williams KM, Prevost AT, et al. Screening for type 2 diabetes and population mortality over 10 years (ADDITION-Cambridge): a cluster-randomised controlled trial. Lancet. 2012;380(9855):1741–1748 | |
Eborall H. Psychological impact of screening for type 2 diabetes: controlled trial and comparative study embedded in the ADDITION (Cambridge) randomised controlled trial. BMJ. 2007;335(7618):486 | |
Quitian H, Aschner P, Muñoz O, Triana Romero PA, Girón D, Gomez-Restrepo C, et al. Economic evaluation of four schemes for screening and diagnosis of type 2 diabetes in adults in Colombia. Value Health. 2015;18(7):A356 | |
Xu N, Wu H, Li D, Wang J. Diagnostic accuracy of glycated hemoglobin compared with oral glucose tolerance test for diagnosing diabetes mellitus in Chinese adults: A meta-analysis. Diabetes Res Clin Pract. 2014;106(1):11–18 | |
Guyatt G, Oxman AD, Akl a E, Kunz R, Vist G, Brozek J, et al. GRADE guidelines: 1. Introduction-GRADE evidence profiles and summary of findings tables. J Clin Epidemiol. 2011;64(4):383–394 | |
King P, Peacock I, Donnelly R. The UK Prospective Diabetes Study (UKPDS): clinical and therapeutic implications for type 2 diabetes. Br J Clin Pharmacol. 1999;48(5):643–648 | |
UK Prospective Diabetes Study (UKPDS) Group. Effect of intensive blood-glucose control with metformin on complications in overweight patients with type 2 diabetes. Lancet. 1998;352(9131):854–865 | |
Wing RR, Bolin P, Brancati FL, Bray AG, Clark JM, Coday M, et al. Cardiovascular effects of intensive lifestyle intervention in type 2 diabetes. N Engl J Med. 2013;369(2):145–154 | |
Sluik D, Buijsse B, Muckelbauer R, Kaaks R, Teucher B, Johnsen NF, et al. Physical activity and mortality in individuals with diabetes mellitus: a prospective study and meta-analysis . Arch Intern Med. 2012;172(17):1285–1295 | |
Umpierre D, Kramer CK, Leita CB, Gross JL, Ribeiro JP, Schaan BD. Physical activity advice only or structured with HbA 1c levels in type 2 diabetes. JAMA. 2011;305:1790–1799 | |
Ajala O, English P, Pinkney J. Systematic review and meta-analysis of different dietary approaches to the management of type 2 diabetes. Am J Clin Nutr. 2013;97:505–516 | |
Estruch R, Ros E, Salas-Salvadó J, Covas M-I, Corella D, Arós F, et al. Primary prevention of cardiovascular disease with a Mediterranean diet. N Engl J Med. 2013;368(14):1279–1290 | |
Phung OJ, Sobieraj DM, Engel SS, Rajpathak SN. Early combination therapy for the treatment of type 2 diabetes mellitus: systematic review and meta-analysis. Diabetes Obes Metab. 2014;16(5):410–417 | |
Wu D, Li L, Liu C. Efficacy and safety of dipeptidyl peptidase-4 inhibitors and metformin as initial combination therapy and as monotherapy in patients with type 2 diabetes mellitus: a meta-analysis. Diabetes Obes Metab. 2014;16(1):30–37 | |
Zhang F, Xiang H, Fan Y, Ganchuluun T-A, Kong W, Ouyang Q, et al. The effects of sulfonylureas plus metformin on lipids, blood pressure, and adverse events in type 2 diabetes: a meta-analysis of randomized controlled trials. Endocrine. 2013;44(3):648–658 | |
Perez A, Zhao Z, Jacks R, Spanheimer R. Efficacy and safety of pioglitazone/metformin fixed-dose combination therapy compared with pioglitazone and metformin monotherapy in treating patients with T2DM. Curr Med Res Opin. 2009;25:2915–2923 | |
Henry RR, Murray AV, Marmolejo MH, Hennicken D, Ptaszynska A, List JF. Dapagliflozin, metformin XR, or both?:: initial pharmacotherapy for type 2 diabetes, a randomised controlled trial. Int J Clin Pract. 2012;66(May):446–456 | |
Lincoff A, Wolski K, Nicholls SJ, Nissen SE. Pioglitazone and risk of cardiovascular events in patients with type 2 diabetes mellitus. JAMA. 2014;298(10):1180–1188 | |
Loke Y, Singh S, Furberg C. Long-term use of thiazolidinediones and fractures in type 2 diabetes: a meta-analysis. CMAJ. 2009;180(1):32–39 | |
Ferwana M, Firwana B, Hasan R, Al-Mallah MH, Kim S, Montori VM, et al. Pioglitazone and risk of bladder cancer: a meta-analysis of controlled studies. Diabet Med. 2013;30(9):1026–1032 | |
Zhang Q, Dou J, Lu J. Combinational therapy with metformin and sodium-glucose cotransporter inhibitors in management of type 2 diabetes: Systematic review and meta-analyses. Diabetes Res Clin Pract. 2014;105(3):313–321 | |
Phung OSJ. Effect of noninsulin antidiabetic drugs added to Metformin therapy on glycemic control, weight gain, and hypoglycemia in type 2 diabetes. JAMA. 2014;303(14):1410–1418 | |
McIntosh B, Cameron C, Singh SR, Yu C, Ahuja T, Welton NJ, et al. Second-line therapy in patients with type 2 diabetes inadequately controlled with metformin monotherapy: a systematic review and mixed-treatment comparison meta-analysis. Open Med. 2011;5(1):e35–e48 | |
Liu S-C, Tu Y-K, Chien M-N, Chien K-L. Effect of antidiabetic agents added to metformin on glycaemic control, hypoglycaemia and weight change in patients with type 2 diabetes: a network meta-analysis. Diabetes Obes Metab. 2012;14(9):810–820 | |
Monami M, Dicembrini I, Kundisova L, Zannoni S, Nreu B, Mannucci E. A meta-analysis of the hypoglycaemic risk in randomized controlled trials with sulphonylureas in patients with type 2 diabetes. Diabetes Obes Metab. 2014;16(9):833–840 | |
Agency for Healthcare Research and Quality. Oral Diabetes Medications for Adults With Type 2 Diabetes: An Update. Comparative Effectiveness Review No. 27. AHRQ Publication No. 11-EHC038-EF. Rockville, MD: U.S. Department of Health and Human Services; 2011. www.effectivehealthcare.ahrq.gov/reports/final.cfm | |
Shyangdan DS, Royle P, Clar C, Sharma P, Waugh N, Snaith A. Glucagon-like peptide analogues for type 2 diabetes mellitus. Cochrane Database Syst Rev. 2011;(10):CD006423 | |
Green JB, Bethel MA, Armstrong PW, Buse JB, Engel SS, Garg J, et al. Effect of Sitagliptin on cardiovascular outcomes in yype 2 diabetes. N Engl J Med. 2015;373(3):232–242 | |
Zannad F, Cannon CP, Cushman WC, Bakris GL, Menon V, Perez AT, et al. Heart failure and mortality outcomes in patients with type 2 diabetes taking alogliptin versus placebo in EXAMINE: a multicentre, randomised, double-blind trial. Lancet. 2015;385(9982):2067–2076 | |
Scirica BM, Bhatt DL, Braunwald E, Steg PGGG, Davidson J, Hirshberg B, et al. Saxagliptin and cardiovascular outcomes in patients with type 2 diabetes mellitus. N Engl J Med. 2013;369(14):1317–1326 | |
Zinman B, Wanner C, Lachin J, Fitchett D, Bluhmki E, Hantel S, Mattheus M, et al. Empagliflozin, cardiovascular outcomes, and mortality in type 2 diabetes. N Engl J Med. 2015;373(22):2117–2128 | |
Quitian H, Aschner P, Muñoz O, Iragorri N, Girón D, Gomez-Restrepo C, et al. Economic evaluation of second line oral antidiabetics for type 2 diabetes in Colombia. Value Health. 2015;18(7):A608–A609 | |
Gross JL, Kramer CK, Leita CB. Effect of antihyperglycemic agents added to Metformin and a Sulfonylurea on glycemic control and weight gain in type 2 diabetes: a network meta-analysis. Ann Intern Med. 2011;154(10):672–679 | |
McIntosh B, Cameron C, Singh SR, Yu C, Dolovich L, Houlden R. Choice of therapy in patients with type 2 diabetes inadequately controlled with metformin and a sulphonylurea: A systematic review and mixed-treatment comparison meta-analysis. Open Med. 2012;6(2):e62–e74 | |
Monami M, Dicembrini I, Nardini C, Fiordelli I, Mannucci E. Effects of glucagon-like peptide-1 receptor agonists on cardiovascular risk: A meta-analysis of randomized clinical trials. Diabetes, Obes Metab. 2014;16(1):38–47 | |
Buehler AM, Cavalcanti AB, Berwanger O, Figueiro M, Laranjeira LN, Zazula AD, et al. Effect of tight blood glucose control versus conventional control in patients with type 2 diabetes mellitus: a systematic review with meta-analysis of randomized controlled trials. Cardiovasc Ther. 2013;31(3):147–160 | |
Miller ME, Williamson J, Gerstein H. Effects of randomization to intensive glucose control on adverse events, cardiovascular disease and mortality in older versus younger adults in the ACCORD Trial. Diabetes Care. 2014;37(3):634–643 | |
Zhang C, Zhou Y-H, Xu C-L, Chi F-L, Ju H-N. Efficacy of intensive control of glucose in stroke prevention: a meta-analysis of data from 59,197 participants in 9 randomized controlled trials. PLoS One. 2013;8(1):e54465 | |
Hemmingsen B, Lund S, Gluud C, Vaag A, Almdal T, Hemmingsen C, et al. Targeting intensive glycaemic control versus targeting conventional glycaemic control for type 2 diabetes mellitus. Cochrane Database Syst Rev. 2013;11:CD008143 | |
Sinclair A, Paolisso G, Castro M, Bourdel I, Gadsby R, Rodriguez L. European Diabetes Working Party for Older People 2011 Clinical Guidelines for Type 2 Diabetes Mellitus ( EDWPOP ). Diabetes Metab. 2011;37(3):s27–s38 | |
International Diabetes Federation. Managing older people with type 2 diabetes. Global guidelines. 2014. Available from: https://www.idf.org/sites/default/files/IDF%20Guideline%20for%20Older%20People.pdf. January 31 2016 | |
Gomez HR. Tratamiento de la diabetes tipo 2 en el paciente anciano. Med Clin (Barc). 2013;140(3):134.e1–134.e12 | |
Turnbull FM, Abraira C, Anderson RJ, Byington RP, Chalmers JP, Duckworth WC, et al. Intensive glucose control and macrovascular outcomes in type 2 diabetes. Diabetologia. 2009;52(11):2288–2298 | |
Anderson RT, Narayan KMV, Feeney P. Effect of Intensive Glycemic Lowering on Health-Related Quality of Life. Diabetes Care. 2011;34:807–812 | |
Mannucci E, Monami M, Lamanna C, Gori F, Marchionni N. Prevention of cardiovascular disease through glycemic control in type 2 diabetes: A meta-analysis of randomized clinical trials. . Nutr Metab Cardiovasc Dis. 2009;19(9):604–612 | |
Lièvre MM, Moulin P, Thivolet C, Rodier M, Rigalleau V, Penfornis A, et al. Detection of silent myocardial ischemia in asymptomatic patients with diabetes: results of a randomized trial and meta-analysis assessing the effectiveness of systematic screening. Trials. 2011;12(1):23 | |
Wackers FJT, Young LH, Inzucchi SE, Chyun DA, Davey JA, Barrett EJ, et al. Detection of Silent Myocardial Ischemia in Asymptomatic Diabetic Subjects: The DIAD study. Diabetes Care. 2004;27(8):1954–1961 | |
Muhlestein JB, Lappé DL, Lima JA, Rosen BD, May HT, Knight S, et al. Effect of screening for coronary artery disease using CT angiography on mortality and cardiac events in high-risk patients with diabetes. JAMA. 2014;312(21):2234 | |
Farmer AJ, Stevens R, Hirst J, Lung T, Oke J, Clarke P, et al. Optimal strategies for identifying kidney disease in diabetes: properties of screening tests, progresion of renal dysfunction and impact of treatment - systematic review and modelling of progression and cost-efectiveness. Health Technol Assess. 2014;18:1–128 | |
Geng DF, Sun WF, Yang L, En G, Wang JF. Antiproteinuric effect of angiotensin receptor blockers in normotensive patients with proteinuria: A meta-analysis of randomized controlled trials. J Renin Angiotensin Aldosterone Syst. 2014;15(107):44–51 | |
Atmaca A, Gedik O. Effects of angiotensin-converting enzyme inhibitors, angiotensin II receptor blockers, and their combination on microalbuminuria in normotensive patients with type 2 diabetes. Adv Ther. 2006;23(4):615–622 | |
Slinin Y, Ishani A, Rector T, Fitzgerald P, MacDonald R, Tacklind J. Management of hyperglycemia, dyslipidemia, and albuminuria in patients with diabetes and CKD: A systematic review for a KDOQI clinical practuce guidelines. Am J Kidney Dis. 2012;60(5):747–769 | |
Haller H, Ito S, Izzo JL, Januszewicz A, Katayama S, Menne J. Olmesartan for the delay or prevention of microalbuminuria in type 2 diabetes. N Engl J Med. 2011;364(10):907–917 | |
National Kidney Foundation. KDOQI Clinical Practice Guideline for Diabetes and CKD: 2012 update. Am J Kidney Dis. 2012;60(5):850–886 |