Introducción
La enfermedad de Gorham-Stout (EGS) u osteolisis esencial, es una enfermedad poco común caracterizada por la proliferación vascular que produce destrucción y resorción de la matriz ósea de etiología desconocida 1.
El primer caso en la literatura de "enfermedad ósea evanescente" como también se conoce a esta patología, fue descrito por Jackson en 1838 en el que se detallaba la desaparición progresiva de un húmero 2. en 1955, Gorham et al., recopilaron una serie de 24 casos propios y otros publicados con similares características clínicas e histológicas 3.aproximadamente, existen unos 185 casos descritos en los que no hay diferencias en cuanto a sexo ni un claro patrón de transmisión hereditaria, pero sí un predominio en la incidencia de la enfermedad durante las primeras décadas de la vida 1. El síntoma inicial más frecuente es el hallazgo de fracturas patológicas, pero en general suelen ser inespecíficos 4, pudiendo afectar cualquier parte del esqueleto, aunque con predilección por los huesos planos como la mandíbula, costillas, hombro y pelvis. La histopatología se caracteriza por la proliferación de un pequeño vaso o un reemplazo de los conductos linfáticos por tejido fibrovascular benigno 1. Suele cursar con un buen pronóstico, mientras que las complicaciones pulmonares secundarias a las lesiones del esqueleto torácico acompañado de quilotórax y el compromiso vertebral son complicaciones poco comunes pero fatales de esta enfermedad 5.
No existe un consenso claro sobre el tratamiento, más adecuado. el tratamiento médico (principalmente el interferón alfa-2b y los bifosfonatos entre los más utilizados), la cirugía con intención de reducir el flujo hacia la cavidad pleural (ligadura del conducto torácico, pleurodesis y pleurectomía), la radioterapia y la quimioterapia (bleomicina y ciclofosfamida principalmente) han sido las opciones que se han probado en casos aislados con diferente éxito 1.
Se presenta un caso de EGS complicado con derrame pleural, en el cual se logró remisión clínica y radiológica con sirolimus con dosis única de carga 4mg y posteriormente dosis de mantenimiento de 1.5 mg/día.
Caso clínico
Mujer de 43 años que ingresó por presentar un dolor torácico, disnea de moderados esfuerzos y tumoración en hipocondrio izquierdo. Dentro de sus antecedentes personales se destacó luxaciones de repetición de hombro derecho desde la infancia y endometriosis diagnosticada dos años antes. Un año antes del ingreso, comenzó con un dolor de características mecánicas en la región esternal, junto con signos inflamatorios, sin traumatismo previo. Seis meses antes del ingreso, presentó un dolor mecánico progresivo en el costado y flanco izquierdo, junto con tumoración en el hipocondrio ipsilateral que fue aumentado lentamente de tamaño y una disnea progresiva hasta ser de moderados esfuerzos. Sin hemoptisis, fiebre, sensación distérmica, escalofríos, tiritona ni otra clínica infecciosa o respiratoria. Tampoco refirió pérdida de peso, astenia ni anorexia. A la exploración se determinó un dolor y un engrosamiento a nivel del décimo arco costal posterior izquierdo, dolor a la palpación en el tercio inferior de la región esternal; y una tumoración difusa en el hipocondrio izquierdo con un hematoma en la superficie y mal delimitada, blanda y no dolorosa. A la auscultación cardiopulmonar presentó semiología de derrame pleural en el campo inferior y medio del hemitórax izquierdo. En las pruebas analíticas al ingreso mostraron un hemograma y bioquímica normales, sin elevación de los reactantes de fase aguda. En la Tabla 1 se pueden observar los datos analíticos al ingreso
| Parámetro | Valor |
|---|---|
| Glucosa | 98 mg/dL |
| Urea | 32 mg/dL |
| Creatinina | 0.63 mg/dL |
| Bilirrubina total | 0.56 mg/dL |
| Proteínas | 7.5 g/dL |
| Albumina | 4.7 g/dL |
| Hemoglobina | 11.9 gr/dL |
| Fibrinógeno | 400 mg/dL |
| Proteina C reactiva | 1.50 mg/dL |
| Osmolaridad | 267 mOsmol/kg. |
| Aspartato aminotransferasa (AST) | 20 UI/L |
| Alanino Aminootransferasa (ALT) | 17 UI/L |
| Fosfatasa alcalina (FA) | 63 UI/L |
| Gammaglutamil transpeptidasa (GGT) | 21 UI/L |
| Lactato deshidrogenasa (LDH) | 157 UI/L |
| Velocidad de sedimentación globular (VSG) | 27 mm |
| Tiempo protrombina | 98% |
| Hematocrito | 34.5% |
| Leucocitos | 6.38 x 10³/μL |
| Plaquetas | 456 x 10³/μL |
| Tiempo de tromboplastina parcial activada | 29.5 s |
| INR | 1.01 |
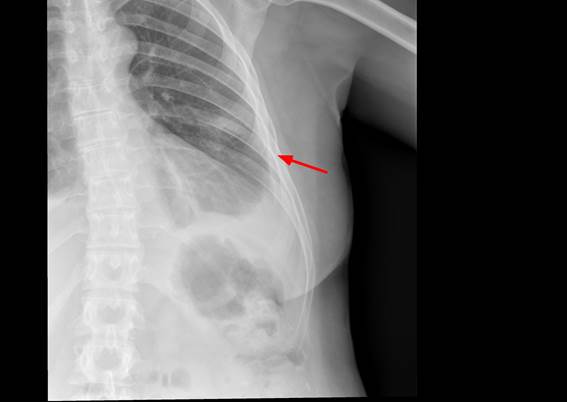
En la radiografía de tórax se apreciaba derrame pleural que ocupaba dos tercios del hemitórax izquierdo y en la parrilla costal izquierda, se intuía una ausencia parcial del 6º arco costal ipsilateral (Fig. 1).
Figura 1
Radiografía de parrilla costal izquierda en la que se intuye desaparición parcial del 6º arco costal lateral y anterior ipsilateral.
Se realizó una toracocentesis evacuadora con salida de líquido de características serohemáticas y que presentó los siguientes datos analíticos: glucosa 97 mg/dL, LDH 179 UI/L, hematíes 571,100/ μL, leucocitos 11,620/ μL (3% polimorfonucleares, 97% mononucleares), proteínas 5.3 g/dL, pH 7.43, factor reumatoide 9.1 UI/mL, amilasa 27 UI/L, colesterol 86 mg/dL, triglicéridos 26 mg/dL, adenosin desaminasa (ADA) 13 UI/L con citometría de flujo del líquido pleural negativa para infiltración linfoide y citología del líquido sin atipias celulares. Los cultivos en líquido pleural para bacterias, micobacterias, parásitos y hongos fueron negativos. Así mismo, la prueba del Mantoux y el test de detección del gamma-interferón mediante la prueba de quantiferon-TB® fueron negativas para infección tuberculosa latente. Las serologías para virus hepatotropos y virus de la inmunodeficiencia humana (VIH), fueron negativas. La mamografía y ecografía ginecológica fueron normales. Tanto en la gammagrafía ósea (Fig. 2) como en la tomografía computarizada, resonancia magnética torácica y tomografía por emisión de positrones (Fig. 3), se observó una hipoplasia y lesión osteolítica en el décimo y el sexto arco costal izquierdo, junto con un derrame, una importante inflamación pleural ipsilateral, y una afectación de partes blandas adyacentes.
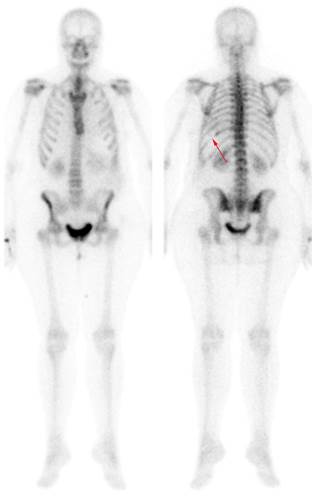
Figura 2
Gammagrafía ósea en la que se aprecia ausencia parcial del 10º arco costal posterior izquierdo.
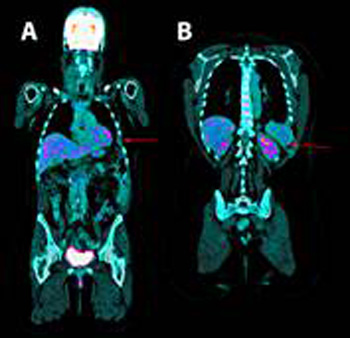
Figura 3
Tomografía por emisión de positrones. A. se aprecia la ausencia del 6º y B. 10º arcos costales izquierdos.
Se realizó toracotomía diagnóstica en la que se apreciaron importantes signos de inflamación e hiperemia pleural, pero sin rasgos de malignidad o granulomas. Se tomaron muestras óseas, pleurales y de parénquima pulmonar. En el resultado histológico del tejido pleural y pulmonar se demostraron hallazgos compatibles con proceso inflamatorio inespecífico. En la biopsia costal, se apreció un proceso inflamatorio crónico, con infiltración fundamentalmente plasmocitoide y tejido de granulación muy artefactado por decalcificación. Ante estos hallazgos y ante la posibilidad de actinomicosis, se inició un tratamiento empírico, inicialmente con penicilina (dosis de 6 millones/UI/6 h durante 4 semanas), a la espera del resultado de la reacción en cadena de la polimerasa para Actinomices sp. Dada la ausencia de mejoría y el resultado negativo para esta prueba, se decidió nuevamente un tratamiento empírico con prednisona a dosis de 1 mg/kg/día. A pesar de todos estos tratamientos y la colocación de un drenaje pleural, la paciente presentó un derrame pleural recidivante; en la última ocasión bilateral, con predominio derecho y una mayor tumoración abdominal. Se determinó el factor de crecimiento endotelial vascular (VEGF) con niveles elevados (287 pg/mL, normal entre 0 y 128.9 pg/mL). En este momento, se revisó de nuevo el caso y a la vista de los hallazgos clínicos, analíticos y radiológicos y aunque no se demostraron inicialmente resultados histológicos compatibles, se diagnósticó EGS y se decidió iniciar un tratamiento con sirolimus tras la firma del paciente del consentimiento informado. Inicialmente a dosis única de 4.0 mg (dosis de carga) y posteriormente a 1.5 mg/día. La respuesta fue muy satisfactoria desde el inicio del tratamiento, con desaparición de la clínica de disnea, dolor y de la tumoración abdominal. Durante 10 meses se mantuvo el tratamiento con niveles de sirolimus alrededor del límite inferior sugerido por el laboratorio (entre 3.8 ng/mL y 4.3 ng/mL; límites: 4 ng/mL mínimo y 10 ng/mL máximo) y controlándose de forma bimensual. Sin embargo, y debido a la sospecha de la relación entre la administración de sirolimus y los episodios de metrorragias abundantes, se decidió suspender el tratamiento. A los pocos días, la disnea, el dolor costal y sobre todo, la tumoración abdominal reaparecieron. Se reinició el tratamiento con sirolimus con remisión completa a la 4° semana y menstruaciones normales. Posteriormente y tras reevaluación de la biopsia, principalmente de las muestras óseas del arco costal, se hallaron zonas de proliferación vascular linfática determinadas con la técnica inmunohistoquímica con el anticuerpo monoclonal D2-40 positiva (de utilidad para el marcaje específico de vasos linfáticos), compatible con el diagnóstico de EGS. Desde entonces y tras dos años del inicio de los síntomas y seguimiento analítico y radiológico a la paciente, esta se encuentra asintomática sin cambios en las pruebas complementarias.
Discusión
En la EGS, la osteolisis masiva y progresiva es producida por la proliferación anormal de capilares endoteliales de origen vascular o linfático. Aunque el mecanismo de reabsorción es desconocido, algunos investigadores han encontrado un aumento en la actividad de los osteoclastos 6,7 junto con una relación con el aumento del VEGF y en otros casos una relación con el aumento de la interleucina 6. En nuestro caso, se pudo constatar una elevación del VEGF que podría servir para el seguimiento y correlacionar con la clínica de la paciente. La EGS se considera que es un diagnóstico de exclusión, con hallazgos clínicos, radiológicos e histopatológicos en ausencia de una causa hereditaria, metabólica, neoplásica, inmunológica o infecciosa, debido a que en la mayoría de los casos no hay hallazgos de laboratorio 8. Radiológicamente los primeros cambios son similares a los de la osteoporosis. En la resonancia magnética se puede observar desaparición de la morfología ósea y áreas de aumento o disminución de la captación, lo que puede causar una hemorragia en diferentes estadios 9. En la paciente que nos ocupa, se llegó al diagnóstico a través de la relación clínica y radiológica con imágenes compatibles con lesiones líticas; tras un razonable descarte de otras patologías de origen neoplásico, infeccioso, inflamatorio o metabólico; y finalmente hallazgos histopatológicos compatibles. Si bien existen una serie de criterios diagnósticos 10 estos son muy poco utilizados entre los autores para el diagnóstico y muchos de ellos abogan más por su uso como diagnóstico de exclusión en el contexto clínico adecuado 1,11,12.
Entre las principales complicaciones de la EGS se encuentran el quilotórax y menos frecuente el derrame pleural serohemático, asociándose estas complicaciones a un aumento de la mortalidad 13.
Existe tratamiento quirúrgico, radioterápico y tratamiento médico. En este último apartado se incluyen principalmente el octreotide, bevacizumab, propranolol, interferón alfa-2b y bifosfonatos (estos dos últimos solos o en combinación, son los más usados); todos ellos con resultados individuales dispares; y por este motivo, ninguno de ellos se ha podido establecer como el tratamiento estándar ante la falta de estudios desarrollados en relación a esta patología.
El Sirolimus, está indicado en la prevención del rechazo de pacientes trasplantados y su mecanismo de acción se debe a que inhibe FK506-binding protein 12-rapamycin-associated protein 1 (FRAP1) con lo que se produce un descenso en la síntesis proteica y por tanto, en la proliferación celular y angiogénesis 14. En este sentido, últimamente se ha probado una alternativa terapéutica con sirolimus en pacientes pediátricos con anomalías vasculares y linfáticas, entre las que se encuentra la EGS, por su papel antiangiogénico, hallándose excelentes resultados 14, por lo que actualmente existe en marcha un ensayo clínico en este grupo de pacientes, con resultados preliminares significativos, motivo por el que se instauró este medicamento en nuestro caso 1,15. Cabe destacar también que la dosis de sirolimus administrada fue a dosis bajas con buena respuesta clínica a pesar de presentar niveles en ocasiones por debajo del nivel inferior sugerido por el laboratorio (4 ng/mL). A diferencia de lo publicado en los otros dos casos, uno con derrame pleural (con niveles alrededor de 9 a 12 mcg/L) 16 y el segundo con afectación exclusivamente ósea (10-15 ng/mL) 17.
Dentro de los efectos secundarios mas frecuentes causados por este medicamento, se encuentran: infecciones (fúngicas, víricas, bacterianas o por Herpes simplex), trombocitopenia, anemia, leucopenia, hipocalcemia, hipofosfatemia, diabetes, hipertensión, trastornos de la menstruación, alteración hepáticas y renales, y aumento del riesgo de aparición de un cáncer, sobre todo linfoma y cáncer de piel 14,15. En nuestro caso la paciente presentó metrorragia, efecto que estuvo ausente al reintroducir el tratamiento. Sin presentar hasta la fecha algún otro efecto secundario. Por último, la recidiva que tuvo ante la suspensión y la respuesta clínica tras la reintroducción del sirolimus, manifiestan un importante papel en el control de la EGS en este caso en concreto.