Nutrición en el nińo cardiópata
Carlos Alberto Velasco, M.D.*
* Profesor Titular, Universidad del Valle. Docente investigador, Universidad Libre Seccional Cali. Docente Universidad Autónoma de Occidente. Director Grupo de Investigación GASTROHNUP, Cali, Colombia. e-mail: cvelasco@univalle.edu.co
Recibido para publicación diciembre 28, 2006 Aceptado para publicación enero 25, 2007
RESUMEN
La clasificación de las enfermedades cardíacas pediátrica, en congénitas y adquiridas, restrictivas y no restrictivas, en cianóticas y no cianóticas, quirúrgicas y no quirúrgicas y agudas y crónicas, ha sido útil para determinar el impacto en el estado nutricional de los nińos. El manejo nutricional del nińo con cardiopatía congénita es complejo, debido a la restricción hídrica, a los elevados requerimientos calóricos y a la prevalencia de intolerancia a los alimentos. A pesar de esto, un estrecho seguimiento y muchos métodos de alimentación son esenciales para obtener unos óptimos resultados médicos, nutricionales y psicosociales.
Palabras clave: Enfermedad cardíaca; Nutrición; Nińos.
Nutrition in congenital heart disease
SUMMARY
Pediatric heart disease classification, in congenital and acquired, restrictive and non-restrictive, cyanotic and non-cyanotic, surgical and non-surgical and acute and chronic, is useful to determine its impact on child’s nutritional status. The nutritional management of CHD children is changing, due to liquid restriction high calorie requirements and high prevalence of food intolerance. Despite this, a close follow-up and several creative feeding methods, are essential to obtain optimal medical, nutritional and psychosocial results.
Keywords: Heart disease; Nutrition; Children.
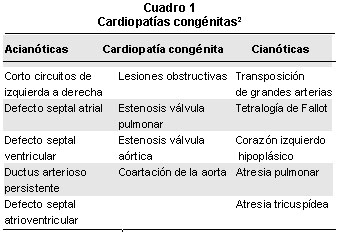
La clasificación de las enfermedades cardíacas pediátricas, en congénitas o adquiridas, en restrictivas o no restrictivas, en cianóticas o acianóticas, en quirúrgicas o no quirúrgicas, y en agudas o crónicas, entre otras, permite determinar el impacto sobre el estado nutricional del nińo que las presenta (Cuadro 1)1,2.
ETIOLOGÍA
Son múltiples los factores de riesgo nutricional para que el nińo cardiópata presente falla para crecer (Cuadro 2)3.
FISIOPATOLOGÍA
Algunos comentarios se relacionan directamente con los factores de riesgo nutricional en el nińo cardiópata: se podría decir que tanto la taquipnea como la taquicardia, pueden de modo significativo incrementar las demandas metabólicas; que en los nińos de las Unidades de Cuidados Intensivos Pediátricos, la disminución del ingreso energético es secundario a su intubación; que la anoxia y congestión venosa del intestino e hígado, con frecuencia se presenta en nińos con falla cardíaca derecha; que la enteropatía perdedora de proteínas está presente luego del procedimiento de Fontan; que las pérdidas renales de electrólitos, son secundarias al uso de diuréticos; y que la disminución de la capacidad gástrica, da como consecuencia, una disminución en el volumen de alimentos por ingerir3. Debido a la neta disminución del consumo de oxígeno en los nińos con insuficiencia cardíaca, toman importancia tanto la acidosis secundaria como el sufrimiento celular4. La reducción en la perfusión sistémica, sobre todo en la circulación esplácnica e intestinal, puede limitar el vaciamiento gástrico, la motilidad intestinal y el aprovechamiento de los nutrientes2.
Cianosis. En general, el nińo cardiópata cianótico, compromete tanto el peso como la talla, mientras que el nińo cardiópata sin cianosis, afecta más el peso que la talla. Asimismo, según la severidad de la hipoxemia asociada con la cianosis, hay variaciones en el grado de retardo en la maduración esquelética3. En general, se entiende, que el ingreso de nutrientes se ve afectado por la fatiga durante la alimentación, secundaria a la hipoxemia2.
Cirugía. En algunas oportunidades, la solución de la cardiopatía que padece el nińo, es quirúrgica, y en estas ocasiones, se requieren intervenciones escalonadas, lo que coloca en riesgo al nińo en falla para crecer, según los intervalos entre cada cirugía3. De allí la importancia de poner en marcha una asistencia nutricional oportuna que impedirá la morbilidad postquirúrgica como infecciones, dificultades en la extubación, cicatrización, etc.4
Enteropatía perdedora de proteínas (EPP) secundaria a cirugía de Fontan. Una de las complicaciones que acompańa a la cirugía de Fontan, es la EPP como albúmina y de otros nutrientes como transferrina, ceruloplasmina, fibrinógeno, lipoproteínas, alfa-1-antitripsina, grasas, minerales, calcio y hierro, entre otros; en la EPP secundaria a la interrupción del flujo linfático y venoso, el nińo se presenta con edema, ascitis, hipoproteinemia y/o linfopenia; y las pérdidas fecales de alfa-1-antitripsina corroboran el diagnóstico. La dieta incluye una dieta hiperproteica, triglicéridos de cadena media, calcio y vitaminas liposolubles3.
DIAGNÓSTICO
La historia clínica se debe enfocar en conocer el tipo de lesión, la edad del diagnóstico, las medicaciones utilizadas (Cuadro 3)5, la capacidad de ser alimentado por vía oral, el tiempo de duración de la alimentación, y la presencia de síntomas agregados durante la alimentación, como diaforesis, entre otras3; así como dirigir una encuesta dietaria por recordatorio de 24 horas, si es el caso, a los padres o tutores que alimentan al nińo, con la idea de realizar una anamnesis desde el punto de vista nutricional (Cuadro 4)6.
La valoración del estado nutricional antropométrico, debe incluir la toma del peso, la talla y el perímetro cefálico, mediante los cuadros del National Center for Health Statistics (NCHS) de los Estados Unidos o los cuadros del Eurogrowth de la Sociedad Europea de Gastroenterología, Hepatología y Nutrición Pediátrica (ESPGHAN), para definir excesos o deficiencias en cuanto se refiere al peso para la edad, la talla para la edad, el peso para la talla, el perímetro para la edad y la talla y el índice de masa corporal (IMC)7, sin olvidar, en algunos nińos, utilizar los cuadros especiales, como en el caso de entidades que con frecuencia acompańan las cardiopatías congénitas como las cromosomopatías del tipo síndrome de Down o el síndrome de Turner, etc.2 Toman igualmente importancia, sobre todo en los nińos que se van a llevar a cirugía, las medidas antropométricas para evaluar el crecimiento como el puntaje zeta, la circunferencia braquial y del triceps2(Cuadro 4)6. En el examen físico hay que buscar la presencia de dedos en palillo de tambor, edema, cianosis, palidez y tomar la frecuencia respiratoria y saturación de oxígeno, al igual que la capacidad para coordinar la succión, deglución y respiración, inclusive cuando se alimenta3; así como la búsqueda de signos que permitan determinar clínicamente el grado de desnutrición del nińo, según la gravedad para clasificarlo como marasmático o kwashiorkor (Cuadro 4)6.
Paraclínicos. Son importantes además de los laboratorios mínimos para evaluar el estado nutricional desde el punto de vista bioquímico, hacer énfasis en la albúmina y en los electrólitos séricos como calcio, magnesio, y fósforo y en los urinarios como sodio, potasio y cloro, cuando el nińo recibe diuréticos3; al igual que un cuadro hemático completo, las pruebas de funcionamiento metabólico, y otras específicas dependientes del déficit nutricional identificado (Cuadro 4)6.
MANEJO
Restricciones hídricas. Es posible que en las formas graves de tipo agudo e incluso en algunas cardiopatías crónicas, sean necesarias reducciones hídricas, hecho sinónimo de restricción calórica4,8, por cuyo motivo, estrategias como el incremento de la densidad calórica bien sea al aumentar la concentración de la fórmula infantil con el mismo polvo, o agregarle módulos de carbohidratos o de grasas, se convierten en una estrategia nutricional para ofrecer, junto con el empleo de diuréticos para evitar las sobrecargas hídricas, y buscar que por lo pronto 1 ml ofrezca como mínimo 1 kilocaloría (1 onza = 30 kilocalorías), con las precauciones de la sobrecarga renal de solutos y el riesgo de deshidratación y disfunción renal, sobre todo si reciben diuréticos2. Ante un lactante que gane más de 50 g/día de peso, se debe sospechar que se puede encontrar retención de líquidos2.
Restricciones sódicas. En general estas restricciones en las cardiopatías crónicas no son necesarias; pero sí en las cardiopatías agudas4, donde se debe tener en cuenta el uso de fórmulas infantiles de iniciación, que son pobres en sodio.
Manejo nutricional. Los nińos con problemas cardíacos requieren calorías adicionales, por ejemplo, en un lactante deben estar por encima de 150 kcal/kg/d y en un nińo mayor, deben ser superiores a 2,500 kcal/m2/d. Ello y según evaluación del estado nutricional y clínico del nińo, mediante la vía enteral, parenteral o ambas; o incluso con la posibilidad de ubicar una gastrostomía9. Todo esto implica una estricta monitorización para evitar excesos o defectos; en países desarrollados se tienen buenas experiencias con el monitoreo por medio del coeficiente respiratorio10 medido por calorimetría indirecta11,12. Las recomendaciones para el soporte nutricional de un nińo con una cardiopatía congénita se resumen en el Cuadro 55.
Nutrición enteral. Sigue siendo válido, que mientras el tubo digestivo esté indenme, ésta sea la primera vía que se ha de utilizar para realimentar estos nińos13. Entre los objetivos de implementar una nutrición enteral temprana, se encuentran: prevenir y evitar la pérdida de masa corporal; fortalecer la respuesta inmune; disminuir y mejorar la retención nitrogenada; conservar la función y la integridad intestinal para evitar y prevenir el sobrecrecimiento bacteriano y así proporcionar un suplemento adecuado de nutrientes a la mucosa digestiva, y atenuar la acidez gástrica con el fin de disminuir el riesgo de úlceras por estrés14-17. Hay algunas circunstancias en el nińo cardiópata que impiden la utilización de esta vía (Cuadro 6)3.
La succión o el paso de sondas naso u orogástricas o yeyunales, o incluso el empleo de gastrostomías parciales o totales9, se convierten en alternativas que se deben tener presentes2, lo que ha permitido ofrecer diversas formas de ostomías, de acuerdo con el momento, el tiempo de permanencia y las condiciones en las que se van a establecer (Cuadro 7)18,19.
Con respecto al tipo de fórmula infantil, hay que tener precauciones ante el riesgo que estos nińos presenten enterocolitis necrosante o sufrimiento intestinal agudo, por lo que es posible que se indiquen2 las fórmulas semielementales con hidrolizados de proteínas (lactoalbúmina o caseína), incluso cuando se ha decidido poner una sonda de alimentación hacia dudodeno/yeyuno/ileón (Cuadro 8)20. En general, la osmolaridad de estas fórmulas infantiles para uso enteral, oscila entre 300 y 650 mOsm/l: se debe anotar, que los nińos presentan síntomas de intolerancia cuando la osmolaridad está por encima de 600 mOsm/l, e incluso hay retardo en el vaciamiento gástrico cuando la osmolaridad duodenal de estas fórmulas es superior a 560 mOsm/l. La densidad calórica de estas fórmulas infantiles está entre 1 y 2 kcal /ml20.
Ya que en general, estas soluciones se pueden convertir en verdaderos cultivos bacterianos, se hace imperiosa la necesidad de ofrecer su adecuada manipulación21.
Nutrición parenteral. Bien sea de manera parcial, o en algunas ocasiones total, o en casa, con sus posibles complicaciones22-24, se debe usar la nutrición parenteral, preferiblemente con soluciones estándar25, sobre todo en circunstancias agudas o en pre o postoperatorios, donde la vía oral está interrumpida o el nińo es incapaz de recibir por vía enteral los nutrientes necesarios para su crecimiento y desarrollo2,13,26 (Cuadro 9)27-29.
CONCLUSIÓN
El manejo nutricional de nińos con cardiopatías es cambiante, debido a las restricciones hídricas, a los elevados requerimientos calóricos y a una alta prevalencia de intolerancia a los alimentos. A pesar de ello, un estrecho seguimiento, y múltiples métodos creativos de alimentación, son esenciales para obtener resultados médicos, nutricionales y psicosociales óptimos.
REFERENCIAS
1. Stockerac CF, Shekerdemian LS. Recent developments in the perioperative management of the paediatric cardiac patient. Curr Opin Anaesthesiol 2006; 19: 375-381.
2. Lewis A, Hsieh V. Congenital heart disease and lipid disorders in children. In: Ekvall SW, Ekvall VK (eds.). Pediatric nutrition in chronic diseases and developmental disorders. Prevention, assessment, and treatment. 2nd ed. Oxford: Oxford University Press; 2005. p. 229-235.
3. Kelleher DK. Cardiac disease. In: Hendricks KM, Duggan C (eds.). Manual of pediatric nutrition. 4th ed. Hamilton: BC Decker; 2006. p. 307-313.
4. Chevallier B. Patologías específicas: nutrición del nińo con cardiopatía. En: Chevallier B (ed.). Manual nutrición infantil. Masson SA: Barcelona; 1997. p. 165-215.
5. Winter H, Madden J. Nutritional support of the chronically ill child. In: Lifschitz CH (ed.). Pediatric gastroenterology and nutrition in clinical practice. New York: Marcel Dekker, Inc.; 2002. p. 399-415.
6. Velasco CA. Nutrición en el paciente pediátrico en estado crítico. En: Velasco CA (ed.). Temas selectos en nutrición infantil. Bogotá: Editorial Médica Distribuna; 2005. p. 205-216.
7. Perrin EM, Flower KB, Ammerman AS. Body mass index charts: useful yet underused. J Pediatr 2004; 144: 455-460.
8. Rogers EJ, Gilbertson HR, Heine RG, Henning R. Barriers to adequate nutrition in critically ill children. Nutrition 2003; 19: 865-868.
9. George DE, Dokler M. Percutaneous endoscopic gastrostomy in children. Tech Gastrointest Endosc 2002; 4: 201-206.
10. Hulst JM, van Goudoever JB, Zimmermann LJ, Hop WC, Buller HA, Tibboel D, et al. Adequate feeding and the usefulness of the respiratory quotient in critically ill children. Nutrition 2005; 21: 192-198.
11. Oosterveld MJS, Van Der Kuip M, De Meer K, De Greef HJMM, Gemke RJBJ. Energy expenditure and balance following pediatric intensive care unit admission: A longitudinal study of critically ill children. Pediatr Crit Care Med 2006; 7: 147-153.
12. Taylor RM, Cheeseman P, Preedy V, Baker AJ, Grimble G. Can energy expenditure be predicted in critically ill children? Pediatr Crit Care Med 2003; 4: 176-180.
13. Shulman RJ, Phillips S. Enteral and parenteral nutrition. In: Lifschitz CH (ed.). Pediatric gastroenterology and nutrition in clinical practice. New York: Marcel Dekker, Inc.; 2002. p. 417-450.
14. Gómez LA. Nutrición enteral en el nińo crítico. En: Quevedo A, Martínez Y, Duque JI, Mejía JA (eds.). El nińo en estado crítico. Fundamentos de pediatría. Medellín: Corporación para Investigaciones Biológicas; 2001. p. 322-327.
15. Briassoulis G, Tsorva A, Zavras N, Hatzis T. Influence of an aggressive early enteral nutrition protocol on nitrogen balance in critically ill children. J Nutr Bioch 2002; 13: 560-569.
16. Atten MJ, Skipper A, Kumar S, Olson DL, Schwenk WF. Enteral nutrition support. Dis Mon 2002; 48: 749-790.
17. Petrillo-Albarano T, Pettignano R, Asfaw M, Easley K. Use of a feeding protocol to improve nutritional support through early, aggressive, enteral nutrition in the pediatric intensive care unit. Pediatr Crit Care Med 2006; 7: 340-344.
18. Jiménez R. Nutrición enteral. En: Velasco CA (ed.). Enfermedades digestivas en nińos. Cali: Programa Editorial Universidad del Valle; 2003. p. 411-429.
19. Jiménez R. Nutrición enteral en la patología digestiva. En: Velasco CA (ed.). Enfermedades digestivas en nińos. 2Ş ed. Cali: Programa Editorial Universidad del Valle; 2006, pp. 567-592.
20. Velasco CA. Soporte nutricional enteral del lactante y nińo mayor. En: Moreno JC, Niederbacher J, Méndez A, García JR, Sosa LM, Latorre F, et al. (eds.). Temas selectos en pediatría. 2Ş ed. Bucaramanga: División de Publicaciones Universidad Industrial de Santander; 2005. p. 409-412.
21. Roy S, Rigal M, Doit C, Fontan JE, Machinot S, Bingen E, et al. Bacterial contamination of enteral nutrition in a paediatric hospital. J Hosp Infect 2005; 59: 311-316.
22. Knafelz D, Gambarara M, Diamanti A, Papadatou B, Ferreti F. Complications of home parenteral nutrition in a large pediatric series. Transp Proc 2003; 35: 3050-3051.
23. Grohskopf LA, Sinkowitz-Cochran RL, Garrett DO, Sohn AH, Levine GI, Siegel JD, et al. A national point-prevalence survey of pediatric intensive care unit-acquired infections in the United States. J Pediatr 2002; 140: 432-438.
24. Suita S, Yamanouchi T, Masumoto N, Ogita K,
Nakamura M, Taguchi S. Changing profile of parenteral nutrition in pediatric
surgery: A 30-year
experience at one institute. Surgery 2002; 131 (Suppl): 275-282.
25. Krohn D, Babl J, Reiter K, Koletzko B. Parenteral nutrition with standard solutions in paediatric intensive care patients. Clin Nutr 2005; 24: 274-280.
26. Velasco CA. Nutrición parenteral en el nińo crítico. En: Velasco CA (ed.). Temas selectos en nutrición infantil. Bogotá: Editorial Médica Distribuna; 2005. p. 169-175.
27. Velasco CA. Nutrición parenteral. En: Moreno JC, Niederbacher J, Méndez A, García JR, Sosa LM, Latorre F, et al. (eds.). Temas selectos en pediatría. 2Ş ed. Bucaramanga: División de Publicaciones Universidad Industrial de Santander; 2005. p. 413-418.
28. Velasco CA. Nutrición parenteral total. En: Velasco CA (ed.). Enfermedades digestivas en nińos. 2Ş ed. Cali: Programa Editorial Universidad del Valle; 2006. p. 593-604.
29. Velasco CA. Nutrición parenteral total ciclada. En: Velasco CA (ed.). Enfermedades digestivas en nińos. 2Ş ed. Cali: Programa Editorial Universidad del Valle; 2006. p. 605-612.
30. Sri Paran T, Corbally M, Fitzgerald RI. New technique for fixation of Broviac catheters. J Pediatr Surg 2003; 38: 51-52.