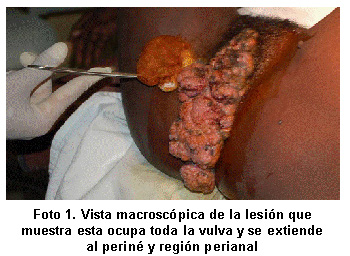
Exéresis quirúrgica radical como único tratamiento del condiloma acuminado gigante: a propósito de un caso*
Indalecio Parapar, M.D.1, Noel Taboada, M.D.2
* Investigación auspiciada por la Brigada Médica Cubana en el Estado de Eritrea, África.
1. Profesor Instructor, Sede Universitaria Yaguajay, Sancti Spiritus, Cuba. e-mail: parapar67@gmail.com
2. Profesor Instructor, Instituto Superior de Ciencias Médicas «Serafín Ruiz de Zárate Ruiz», Villa Clara, Cuba. e-mail: noeltbd@yahoo.com
Recibido para publicación agosto 24, 2006 Aceptado para publicación abril 16, 2007
RESUMEN
Los condilomas o verrugas genitales son producidos por el virus del papiloma humano del que existen más de 100 genotipos distintos. De ellos, cerca de 40 son transmitidos sexualmente. Se presenta el caso de una mujer con condiloma acuminado gigante de localización vulvo perineal y perianal, de cinco ańos de evolución que le dificultaba la micción, las relaciones sexuales, e incluso la marcha; además había fetidez, prurito y en ocasiones dolor. El examen histopatológico fue compatible con condiloma acuminado. Se realizó extirpación quirúrgica radical del tumor con excelentes resultados funcionales y cosméticos, sin complicaciones postoperatorias y sin recurrencias ni cicatrices hipertróficas al ańo de evolución. Es de interés la publicación por tratarse del primer caso que se informa en el Estado de Eritrea, país en desarrollo del cuerno africano.
Palabras clave: Verrugas genitales; Cirugía menor; Resultado del tratamiento.
Surgical radical excision alone as a treatment for the giant condyloma acuminatum: a case report
SUMMARY
Condylomas or genital warts are caused by the human papilloma virus, from which exist more than 100 different genotypes. About 40 of them are sexually transmitted. We report a case of a female patient with a giant condyloma acuminatum in the vulvar perineal and perianal regions, of around five years of course, which disturbs her urination, sexual intercourse, and even walk; accompanied by pruritus, foul-smelling, and occasionally pain. The histopathological study was compatible with condyloma acuminatum. She was treated conservatively with radical local surgical excision of the tumor with excellent functional and cosmetic results. No postoperative complications were observed. A year later there were neither recurrences nor hypertrophic scars. We consider interesting to publish it due to it’s the first case published in the state of Eritrea, developing country of the horn of Africa.
Keywords: Warts genital; Minor surgery; Treatment outcome.
Los condilomas o verrugas genitales son producidos por el virus del papiloma humano (VPH), del que existen más de 100 genotipos, en más de 80 ha sido posible secuenciar por completo su genoma. De ellos, cerca de 40 se transmiten sexualmente e infectan el aparato genital masculino y femenino.
Los VPH son virus de 50 a 55 nm de diámetro, de forma icosahédrica con 72 capsómeros que rodean un ADN de doble cadena circular con casi 8,000 pares de bases, que presentan dos modos de replicación, una replicación estable del genoma viral en las células basales y otra conocida como vegetativa que ocurre en las células más diferenciadas para generar progenies de virus. Aunque todas las células afectadas contienen el genoma viral, la expresión de los genes virales se vincula estrechamente con la diferenciación celular. Casi todos los genes virales se activan cuando los keratinocitos infectados sobrepasan la membrana basal. La producción de las partículas víricas ocurre sólo en los keratinocitos altamente diferenciados, por tanto, la replicación de los virus ocurre tan sólo en la superficie epitelial donde las células están en mayor contacto con factores ambientales.
Las lesiones típicas de los VPH surgen de la proliferación de los keratinocitos basales infectados. La infección típicamente ocurre cuando las células basales del huésped se exponen a la infección viral a través de una barrera epitelial dańada, como sucede durante el acto sexual o como producto de otras abrasiones dérmicas menores. La replicación viral se confina al núcleo celular, y, en consecuencia, las células infectadas exhiben un alto grado de atipia nuclear1.
Según la posibilidad que tienen de provocar lesiones cancerígenas, los VPH se dividen en dos grandes grupos: alto y bajo riesgo.
Se denomina factor de riesgo al que se asocia con el peligro de desarrollar una enfermedad pero sin suficiente compromiso para causarla. Se necesita la presencia de otros factores asociados para producir la enfermedad (que en el caso del VPH son: conducta sexual inadecuada, mala nutrición, tabaquismo, multiparidad, depresión del sistema inmunológico y uso prolongado de anticonceptivos orales).
Los VPH de bajo riesgo son aquellos cuya relación para provocar cáncer es baja, como los serotipos VPH 6, 11, 40, 42, 53, 54 y 57.
Los VPH de alto riesgo son los que se encuentran con mayor frecuencia asociados en los casos de cáncer de cuello uterino e incluyen el VPH 16, 18, 31, 35, 39, 45, 51, 52, 56 y 58. De estos tipos el VPH 16 y el 18 son, sin duda, los más oncogénicos al encontrarse más comúnmente vinculados con el cáncer cérvicouterino2.
El genoma de los HPV consiste en un ADN circular, separado del núcleo celular del huésped en las infecciones de VPH de bajo riesgo, como en los casos que se asocian con los VPH 6 y 11; por su parte el genoma de los VPH de alto riesgo se integra de modo típico con el ADN nuclear del huésped en las lesiones malignas. Precisamente esta integración del genoma viral con el genoma del huésped se considera como una característica distintiva de la transformación maligna. Las proteínas virales E6 y E7 de los serotipos de alto riesgo inactivan las proteínas supresoras tumorales p53 y Rb del huésped, lo que lleva a una proliferación celular incontrolada y a la transformación maligna1.
Los condilomas acuminados (CA) constituyen una de las enfermedades de transmisión sexual más frecuentes y se vinculan por lo general con los tipos de cepas número 6 y 113.
En raras ocasiones los CA pueden evolucionar como un tumor invasivo con malignidad local, aunque sin metástasis, equivalente a un carcinoma verrucoso: es el síndrome de Bruschke-Löwenstein o condilomatosis precancerosa de Delbaco y Unna4.
El CA gigante o tumor de Buschke-Löwenstein es un gran tumor en forma de coliflor, de crecimiento lento, e infrecuente que afecta la región anogenital, que a pesar de un tipo histológico benigno se comporta de forma maligna, con infiltración de los tejidos adyacentes, un alto índice de recurrencia y transformación ocasional hacia el carcinoma de células escamosas, causado por los VPH tipos 6 y 11 y en ocasiones por los tipos 16 y 184-7.
Eritrea es un país en desarrollo ubicado en el cuerno este de África; es étnicamente heterogéneo, pues allí conviven las etnias Tigrinya, Tigre, Saho, Nara, Hedareb, Beja, Afar, Bilen, Kunama y Rashaida, cada una con un dialecto nativo distinto8. Como es el primer caso que se informa en Eritrea, es de interés su publicación.
Para efectuar este trabajo se tuvieron en cuenta los principios éticos de la confidencialidad de la identidad personal, el consentimiento informado, la beneficencia y la no maleficencia en el proceder terapéutico. En este caso se solicitó el consentimiento de la paciente para la publicación del artículo, se le garantizó que se omitirían todas las referencias de datos personales que permitiesen su identificación, así como que las fotos se circunscribirían apenas a la región anatómica donde se ubica la lesión, y se evitaría en todo momento mostrar el rostro; las fotografías siempre se tomaron en presencia de un personal médico y/o paramédico del sexo femenino. Como en el Estado de Eritrea no hay un comité de ética que evalúe los trabajos científicos de los colaboradores de la Brigada Médica Cubana fue imposible contar con la aprobación respectiva.
CASO CLÍNICO
Mujer de 24 ańos de edad, de la etnia Tygrinya, sin antecedentes patológicos personales ni familiares de interés, menarquia a los 12 ańos, primeras relaciones sexuales a los 18 ańos. Nulípara, nunca se ha hecho prueba de Papanicolaou, acude a consulta y refiere que desde hace aproximadamente cinco ańos comenzó a presentar lesiones en forma de verrugas a nivel de la vulva y región perianal que aumentaron en número y volumen hasta fundirse en una verruga genital de gran tamańo, que le dificulta la micción, las relaciones sexuales, incluso la marcha, acompańada de fetidez, prurito y en ocasiones de dolor.
Al examen físico se constata una enorme lesión papilomatosa vegetante con secreción fétida, de aspecto tumoral, que ocupa toda la vulva y se extiende a todo el periné (Foto 1).
Exámenes complementarios: Hemograma completo: Hb 10.8%, leucocitos 10.6 x 109 (P-076, L-024, E-001), eritrosedimentación 50 mm/h, serología (VDRL) no reactiva, VIH negativo, glicemia 3.3 mmol/l, antígeno superficie negativo, antígeno hepatitis C negativo. Ultrasonido ginecológico: compatible con la normalidad. En el estudio histopatológico se observa hiperqueratosis, acantosis y vacuolización citoplasmática (koilocitosis), compatible con CA (Foto 2).
Se hizo remoción quirúrgica total de la lesión con excelentes resultados funcionales y cosméticos. No hubo complicaciones en el postoperatorio mediato (Foto 3), ni en el inmediato, según las valoraciones a las cuatro semanas (Foto 4) y a las seis semanas (Foto 5). Al ańo de intervenida no se constataron recidivas, ni cicatrices hipertróficas deformantes.
DISCUSIÓN
En el mundo la mayor frecuencia de VPH de alto riesgo se encuentran en África y América Latina. En mujeres jóvenes la frecuencia de infección con el VPH es muy alta: hasta 50% de las mujeres adolescentes y adultas jóvenes adquieren la infección en los primeros 4 a 5 ańos de una vida sexual activa2. Aproximadamente 20 millones de personas están infectadas en la actualidad con el VPH1.
El CA gigante presenta características clínicas de malignidad, pero histológicamente, es un tumor benigno. Se manifiesta en la clínica por lesiones verrugosas, exofíticas, gigantes y de comportamiento invasor, con rápido crecimiento y destrucción de estructuras vecinas. Aparece en múltiples localizaciones anatómicas. En los hombres suelen localizarse sobre todo en el pene (81% a 94%), en la región ano rectal (10% a 17%) y uretra (5%). En las mujeres la localización es esencialmente vulvar (90%), aunque también puede verse en la región ano rectal6, hay otras más infrecuentes como la vejiga, e incluso la región oral7.
El rápido desarrollo de los condilomas gigantes suele estar ocasionado por un deficiente estado inmunitario del paciente, en asocio con inmunodeficiencias congénitas y adquiridas como sida, tratamiento inmunosupresor, alcoholismo, y diabetes melitus, factores que se descartaron en este caso según el interrogatorio y los resultados de los exámenes complementarios realizados. También se describen factores predisponentes como mala higiene, promiscuidad, preexistencia de recidivas de vegetaciones venéreas y otros cofactores carcinogénicos6,9.
La paciente comenzó su vida sexual activa a los 18 ańos de edad, y refiere una sola pareja sexual hasta la fecha. Se considera a la conducta sexual como el principal factor de riesgo para la infección con el VPH. Aumentan el riesgo el inicio precoz de relaciones sexuales, antes de los 20 ańos y el número de compańeros sexuales. Se ha demostrado la presencia de VPH cervical o vulvar en 17% a 21% de las mujeres con una pareja sexual y en 69% a 83% de las mujeres con 5 ó más parejas sexuales. Es importante tener en cuenta que la promiscuidad sexual del hombre también constituye un factor de riesgo, pues en sus múltiples contactos sexuales se infecta con VPH que trasmite después a su pareja2.
A la mayoría de las mujeres se les diagnostica el VPH con base en los resultados anormales en las pruebas de Papanicolaou. Este examen citológico es la herramienta primaria de detección del cáncer cervical o cambios pre-cancerosos en el cuello uterino, muchos de los cuales se relacionan con el VPH. Existe además una prueba específica para descubrir el VPH en el ADN de las mujeres (prueba de ADN del VPH). La prueba puede realizarse en mujeres con resultados anormales leves en las pruebas de Papanicolaou o en mujeres mayores de 30 ańos de edad en el momento de hacer la prueba de Papanicolaou. Los resultados de la prueba de ADN del VPH pueden ayudar a los proveedores de atención médica a decidir si se necesitan pruebas o tratamientos adicionales1.
No se recomienda tratamiento para la mayoría de las infecciones por VPH, excepto para aquellos casos en que haya CA visible, o alteraciones en la prueba de Papanicolaou. No existe ningún medicamento capaz de destruir el VPH, el tratamiento está dirigido a extirpar el tejido alterado, ya sean los CA, la anormalidad celular precancerosa, o el cáncer en sí. Si bien se eliminen o se destruyan esas lesiones, el VPH persiste con frecuencia en las áreas adyacentes. Aunque los síntomas del VPH se pueden tratar, la infección del VPH en sí misma no puede ser curada. La mayoría de los condilomas pueden desaparecer espontáneamente, aun sin tratamiento.
Entre los tratamientos tópicos para el CA se encuentra el podofilox y el imiquimod. Ambas son cremas para aplicar a los CA. El primero produce destrucción del CA, y el segundo actúa al estimular el sistema inmune del organismo, y en consecuencia destruye el CA. Otras técnicas terapéuticas incluyen la crioterapia, casi siempre mediante el uso de nitrógeno líquido, que constituye un excelente tratamiento de primera línea, en particular para las lesiones perianales. Otros agentes como el ácido tricloroacético y la resina de podofilina también se pueden usar en la consulta médica. Para algunos CA, sobre todo los de mayor tamańo, se prefiere la escisión quirúrgica, o la destrucción por electrocauterización o tratamiento láser3,10.
En el caso del CA gigante o tumor de Buschke-Löwenstein el tratamiento es tema de controversias; se considera que el de primera línea es la remoción quirúrgica radical, que logra un promedio de éxito entre 63% y 91% y bajo nivel de recurrencia4,7-12. Sin embargo, algunos especialistas consideran que este manejo se debe combinar con quimioterapia10,13 y otros han logrado resultados satisfactorios con la electrocauterización solamente14, o por tratamiento quirúrgico combinado de escisión-vaporización mediante cirugía láser de dióxido de carbono15.
En el ańo 2006, la Agencia Reguladora del Medicamento (Food and Drug Administration, FDA) de Estados Unidos de América (EUA) y el Comité Asesor para la Inmunización y Vacunación (Advisory Committee on Immunization Practices, ACIP) del Centro para el Control de Enfermedades (Center for Disease Control and Prevention, CDC) aprobaron y regularon la utilización de la primera vacuna cuadrivalente, que contiene antígenos de dos genotipos de alto riesgo (16 y 18), responsables de 70% de los cánceres de cuello uterino, y dos de bajo riesgo (11 y 6), responsables de 90% de las verrugas genitales y de la papilomatosis respiratoria recurrente. La Agencia Europea de Regulación de Medicamentos (European Agency for the Evaluation of Medicinal Products, EMEA) ha autorizado el producto recientemente y la autorización en los estados miembros parece inminente. La EMEA también evalúa una segunda vacuna bivalente, que contiene antígenos de los genotipos 16 y 18.
El principio fundamental de estas vacunas es la inhibición de la entrada del virus a la célula hospedera, usualmente mediante la inducción de anticuerpos neutralizantes. En el caso del VPH, en la década de 1990 se logró la producción in vitro de las virus-like particles (VLP) o partículas similares al virus, las cuales son estructural y antigénicamente similares a los viriones nativos pero que no contienen el genoma del virus y, por tanto, carecen de la capacidad para replicarse, causar infección y, mucho menos, cáncer. Estas partículas se producen mediante la expresión del gen L1, que codifica para la proteína mayor de la cápside, en sistemas recombinantes como baculovirus, levaduras y bacterias.
Los ensayos clínicos controlados y aleatorios han demostrado que ambas vacunas son eficaces, seguras e inmunogénicas, pues no producen efectos adversos serios e inducen una fuerte respuesta humoral con títulos de anticuerpos neutralizantes mucho más altos que los inducidos por una infección natural.
Un elemento importante que se debe considerar en la introducción de estas vacunas en los países pobres, que son los que más las necesitan, es el precio. En EUA y Europa el precio de catálogo de las tres dosis de la vacuna cuadrivalente es de US $360, lo cual resulta prohibitivo para las naciones pobres.
Los buenos programas basados en citología han sido difíciles de organizar en los países en desarrollo; en estos países se debe, entonces, considerar estrategias nuevas basadas en baja tecnología, como la inspección visual con ácido acético o lugol o las nuevas pruebas rápidas y baratas de detección de VPH que el Programa de Tecnologías Apropiadas en Salud (Program of Appropriate Technology in Health, PATH) está desarrollando y que planea evaluar el próximo ańo en India y China. El uso de una de estas pruebas seguido inmediatamente por el tratamiento de las lesiones precancerosas detectadas, junto con la vacunación de las adolescentes y las mujeres jóvenes, podría ser la solución ideal para los países en vías de desarrollo16,17.
REFERENCIAS
1. Gearhart PA, Randall TC, Buckley RM. Human papillomavirus. [en línea]. [fecha de acceso enero 11 de 2007]. URL disponible en: http://www.emedicine.com/med/topic1037.htm
2. Muńoz RC. Epidemiología del virus del papiloma humano. [en línea]. [fecha de acceso enero 11 de 2007]. URL disponible en: http://geosalud.com/VPH/epivph.htm
3. Pérez ER, Crespo CG, Isla A, Velazco A. Condiloma gigante de Bushke y Loewenstein a propósito de 2 casos. Rev Cubana Obstet Ginecol 2005; 31: 101-107.
4. Montero VMP, Batallán JMP, Batista MN, Dager HA. Condiloma acuminado gigante. Presentación de un caso. Correo Cient Med Holguin 2004; 8: 81-87.
5. Tytherleigh MG, Birtle AJ, Cohen CE, Glynne-Jones R, Livingstone J, Gilbert J. Combined surgery and chemoradiation as a treatment for the Buschke-Löwenstein tumour. Surgeon 2006; 4: 378-383.
6. Machado CI, Castillo OA, Ochoa OMC, García GR, Lamar MY. Condiloma gigante de Buschke y Lowenstein. A propósito de un caso. Dermatol Peru 2006; 16:74-76.
7. De Toma G, Cavallaro G, Bitoni A, Polistena A, Onesti MG, Scuderi N. Surgical management of perianal giant condyloma acuminatum (Buschke-Löwenstein tumor). Report of three cases. Eur Surg Res 2006; 38: 418-422.
8. Eritrea. From Wikipedia. [en línea]. [fecha de acceso abril 2 de 2007]. URL disponible en: http://en.wikipedia.org/wiki/Eritrea#Demographics
9. Gupta RR, Puri Up, Majan BB, Garg G. Intraoral giant condyloma acuminatum. Indian J Dermatol Venereol Leprol 2001; 67: 264-265.
10. Ambriz GG, Escobedo ZL, Carrillo DM, Ortiz AA, Cordero ZA, Corona NA, et al. Buschke-Lowenstein tumor in childhood: a case report. J Pediatr Surg 2005; 40: 25-27.
11. Delaram G. Condyloma acuminata. [en línea]. [fecha de acceso enero 18 de 2007]. URL disponible en: http://www.emedicine.com/EMERG/topic107.htm
12. Parise P, Sarzo G, Finco C, Marino F, Savastano S, Merigliano S. Giant condyloma acuminatum of the anorectum (Buschke-Lowenstein tumor): a case report of conservative surgery. Chir Ital 2004; 56: 157-161.
13. Tytherleigh MG, Birtle AJ, Cohen CE, Glynne-Jones R, Livingstone J, Gilbert J. Combined surgery and chemoradiation as a treatment for the Buschke-Lowenstein tumour. Surgeon 2006; 4: 378-383.
14. Renzi A, Brusciano L, Giordano P, Rossetti G, Izzo D, Del genio A. Buschke-Löwenstein tumor. Successful treatment by surgical electrocautery excision alone: a case report. Chir Ital 2004; 56: 297-300.
15. Frega A, Stentella P, Tinari A, Vecchione A, Marchionni M. Giant condyloma acuminatum or Bushke-Lowenstein tumor: review of the literature and report of three cases treated by CO2 laser surgery. A long-term follow-up. Anticancer Res 2002; 22: 1201-1204.
16. Bosch FX, Bernaola EI. La vacuna frente al virus del papiloma humano y la incorporación de la pediatría a la prevención del cáncer de cuello uterino. An Pediatr 2006; 65: 411-413.
17. Muńoz N. New perspectives for cervical cancer prevention based on human papiloma virus. Biomedica 2006; 26: 471-474.