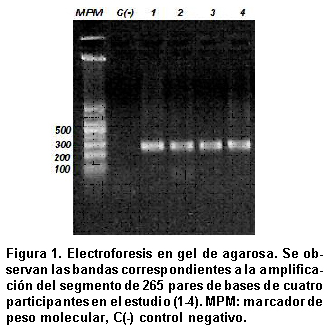
Evaluación del efecto de cuatro polimorfismos en el gen del receptor adrenérgico β-2 en el parto pretérmino
Juan Carlos Ríos, MD1, Juan Guillermo McEwen, MD, PhD2, Adriana Cuartas, MD3, Fanny Cuesta, Ing Quim4, Sergio Parra, MD5
1. Postdoctoral Fellow, University of Houston, USA. e-mail: jcriost@yahoo.com
2. Jefe Unidad de Biología Celular e Inmunogenética, Corporación para las Investigaciones Biológicas (CIB). Profesor Titular, Facultad de Medicina, Universidad de Antioquia, Medellín, Colombia. e-mail: mcewen@une.net.co
3. Profesora Asociada, Departamento de Ginecología y Obstetricia, Facultad de Medicina, Universidad de Antioquia, Medellín. e-mail: adrimacu@gmail.com
4. Profesora Titular (j), Departamento de Farmacología y Toxicología, Facultad de Medicina, Universidad de Antioquia, Medellín. e-mail: fcuesta@quimbaya.udea.edu.co
5. Profesor Aspirante, Departamento de Farmacología y Toxicología, Facultad de Medicina, Universidad de Antioquia, Medellín. e-mail: sparra@quimbaya.udea.edu.co
Recibido para publicación junio 14, 2007 Aceptado para publicación enero 31, 2008
RESUMEN
Objetivo: Determinar si los polimorfismos de nucleótido único encontrados en la secuencia del receptor β-2 adrenérgico β2AR) se asocian con el parto pretérmino espontáneo.
Método: Se realizó un estudio de casos y controles no pareado en el que se determinaron y compararon las frecuencias alélicas, genotípicas y haplotípicas de cuatro polimorfismos, -47 C/T, -20 C/T, Arg16Gly y Gln27Glu del gen del β2AR, entre 35 mujeres con parto pretérmino (casos) y 105 mujeres con parto a término (controles). El estudio se hizo con pacientes de tres instituciones hospitalarias de la ciudad de Medellín, Colombia. Se aisló el ADN genómico de sangre periférica, se amplificó el segmento del gen mediante la reacción en cadena de la polimerasa (PCR) y se determinaron los polimorfismos por secuenciación directa.
Resultados: No se encontraron diferencias significativas de las frecuencias alélicas de los loci polimórficos -47 C/T, -20 C/T, Arg16Gly y Gln27Glu entre el grupo de casos (21.5%, 21.5%, 51.5% y 21.5%, respectivamente) y los controles (21.5%, 21.5%, 57% y 21.5%, respectivamente (p>0.05). Las frecuencias genotípicas también fueron similares entre las pacientes con parto pretérmino y las de parto a término (p>0.05 para todos los genotipos). De los 16 posibles haplotipos, resultantes de la combinación entre los distintos alelos, sólo se presentaron tres en toda la población de estudio (CCGG, TTGC, TTAC). Las frecuencias haplotípicas tampoco tuvieron diferencias significativas entre los grupos comparados (p>0.05).
Conclusión: No se observó una asociación entre el parto pretérmino y cualquiera de los polimorfismos o sus haplotipos. Estos resultados no apoyan una participación de los polimorfismos del β2AR en el trabajo de parto pretérmino espontáneo en estas pacientes.
Palabras clave: Polimorfismo; Parto pretérmino; Receptores adrenérgicos β-2; Alelos; Haplotipos.
Role of four polymorphisms of the β-2 adrenergic receptor gen in patients with preterm delivery
SUMMARY
Objective: To determine whether single nucleotide polymorphisms found in the sequence of the β-2 (β2AR) adrenergic receptor are associated with spontaneous preterm delivery.
Method: A case-control study in which the allelic, genotype, and haplotype frequencies of four polymorphisms, -47 C/T, -20 C/T, Arg16Gly, and Gln27Glu of the β2AR gene, were determined and compared between 35 women with preterm delivery (cases) and 105 women with term delivery (controls). The study was performed with patients of three hospitals in the city of Medellín, Colombia. The genomic DNA of peripheral blood was isolated, the segment of the gene was amplified by means of the chain reaction of polymerase (PCR), and the polymorphisms were determined by direct sequence method.
Results: No significant differences for the allelic frequencies were found for polymorphic loci -47 C/T, -20 C/T, Arg16Gly, and Gln27Glu between the cases group (21.5%, 21.5%, 51.5% and 21.5%, respectively) and controls (21.5%, 21.5%, 57% and 21.5%, respectively; p>0.05). The genotype frequencies were also similar between patients with preterm delivery and those with term delivery (p>0.05 for all the genotypes). Only three of the 16 possible haplotypes (CCGG, TTGC, and TTAC), from the combination between the different alleles, appeared in the participants of this study. The haplotype frequencies were not significantly different between the compared groups either (p>0.05).
Conclusion: No association was observed between preterm delivery and any of the polymorphisms or its haplotypes. These results do not support a role of the polymorphisms of the β2AR in spontaneous preterm delivery for these patients.
Keywords: Polymorphism; Preterm delivery; β-2 adrenergic receptors; Alleles; Haplotypes.
El parto pretérmino es la causa más importante de mortalidad y morbilidad neonatal, y es el responsable de casi 70% de las muertes neonatales, con una prevalencia estable por más de tres décadas1, 2, 3. Miles de niños en el mundo nacen cada año antes de alcanzar el término, lo que representa un elevado índice de complicaciones y secuelas para el recién nacido. Aunque los adelantos científicos y tecnológicos en cuidados neonatales han logrado aumentar la sobrevida aun en recién nacidos a edades gestacionales muy tempranas, no han mostrado un impacto positivo en la morbilidad a largo plazo4.
En el parto pretérmino, una enfermedad multifactorial, se consideran diferentes factores causales como la infección, las alteraciones endocrinas, la hemorragia, la sobredistensión uterina, los factores socioeconómicos y otros aspectos ambientales. A su vez, la naturaleza recurrente del parto pretérmino5, 6, la distinta frecuencia de presentación entre las razas7, 8, 9 y la fuerte agregación familiar que se ha evidenciado en algunos estudios10, 11, hace pensar que los factores genéticos también podrían cumplir un papel importante en su etiología12.
La variabilidad genética podría estar representada en este caso por algunos polimorfismos de proteínas comprometidas en la actividad contráctil del útero humano, lo que influiría sobre la frecuencia de presentación del parto pretérmino o incluso podría alterar la respuesta a los fármacos que se utilizan en la amenaza de parto pretérmino. Entre los candidatos para estudios de asociación genética con el parto pretérmino se han estudiado los genes de varias citoquinas proinflamatorias (factor de necrosis tumoral a, interleuquinas 1 y 6, etc.)13, 14, 15, de la oxido nítrico sintasa y de los receptores β-2 adrenérgicos (β2AR)16, 17, 18, 19.
Los β2AR, que pertenecen a la superfamilia de receptores acoplados a la proteína G20, se consideran como el principal mecanismo de comunicación intercelular para inducir relajación de las fibras musculares miometriales21. Cuando se produce la unión del β2AR con sus ligandos, la adenilato ciclasa aumenta la concentración de adenosil monofosfato cíclico (cAMP) intracelular, se activa la proteína quinasa A (PKA), que inhibe la quinasa de las cadenas ligeras de miosina por medio de la fosforilación22 (esta última cuando se encuentra en su estado activado favorece la contracción muscular). A su vez, la estimulación de los β2AR produce activación de canales de potasio con hiperpolarización de los miocitos uterinos23. Tanto las vías de señalización intracelular como la expresión y el número de β2AR sufren alteraciones importantes en relación con el comienzo del trabajo de parto24, 25, al parecer para minimizar una oposición relajante fisiológica.
El β2AR es una proteína de 413 aminoácidos, producto de un gen sin intrones localizado en el brazo largo del cromosoma 5, con una región codificante de 1239 pares de bases26. De los múltiples polimorfismos en su gen sólo existen algunos que modifican su función. Entre ellos los más comúnmente encontrados se localizan en las posiciones -47, -20, 46 y 79. El polimorfismo de la base -47 consiste en un cambio de una citosina por una timina (-47 C/T), y ocasiona el reemplazo del aminoácido arginina por cisteína (Arg por Cys) en el aminoácido 19 de un péptido que regula la expresión del receptor27, 28. La variante de la base -20 (-20 C/T) es un polimorfismo silencioso, que no modifica la secuencia de aminoácidos, pero que presenta un fuerte desequilibrio de ligamiento con los de las posiciones -47 y 7929. En el polimorfismo del nucleótido 46 se encuentra un cambio de adenina por guanina (A por G), que produce la sustitución de una arginina por una glicina en el aminoácido 16 del β2AR (Arg16Gly). La variante encontrada en la posición 79 (C por G) codifica para el aminoácido 27 del receptor, donde se observa un cambio de la glutamina por el ácido glutámico (Gln27 Glu)30, 31.
Existe evidencia in vitro de que las variantes genéticas mencionadas alteran los procesos de desensibilización y regulación del número de receptores32, 33, mientras que in vivo se informó que influyen la respuesta a sus ligandos en diversos tejidos34, 35.
Se ha encontrado que la homocigocidad para el polimorfismo Arg16, asociada con la atenuación del proceso de disminución del número de los β2AR in vitro, protege del parto pretérmino17, y que el alelo Glu27, que se asocia con resistencia a la desensibilización in vitro, contradictoriamente podría ser un factor de riesgo para el parto antes de las 37 semanas de gestación18.
Según la hipótesis de este estudio, la presencia de uno o varios de estos polimorfismos genéticos de los β2AR podrían ser un factor asociado con la presentación del parto pretérmino.
MATERIALES Y MÉTODOS
Pacientes. La población de estudio consistió de 140 mujeres colombianas, que terminaron sus embarazos en el Hospital General de Medellín, el Hospital Universitario San Vicente de Paúl o la Clínica del Prado de la ciudad de Medellín. Los comités de ética del Centro de Investigaciones Médicas de la Universidad de Antioquia y de las tres instituciones hospitalarias aprobaron el estudio que se llevó a cabo con los lineamientos de la declaración de Helsinki y la Resolución 8430 de 1990 del Ministerio de Protección Social de Colombia. Sólo se incluyeron mujeres hispanas de fenotipo mixto (color de piel trigueño), pues la frecuencia de los polimorfismos del β2AR varía con la etnicidad29, con embarazo único, sin evidencia de infección genitourinaria o sistémica, sin malformaciones uterinas ni anomalías fetales, sin ruptura prematura de membranas ovulares, sin historia de abuso de alcohol o drogas ilícitas, sin presencia de enfermedades ni uso crónico de medicamentos. Los diferentes criterios de exclusión aplicados fueron aquellos que tenían:
1. Implicaciones en el establecimiento de un diagnóstico claro (fecha de la última menstruación no confiable o edad gestacional confusa).
2. Relación con la presentación del parto pretérmino, distintas frecuencias de los polimorfismos o complicaciones concomitantes (antecedente de TPP en la gestación actual tanto para pacientes como para controles, antecedente de TPP en embarazos previos para los controles, ruptura de membranas, embarazo múltiple, raza negra, corioamnionitis y otras infecciones, arritmias, disautonomías, hipertensión, enfermedad coronaria, enfermedad valvular o cardiomiopatías, daño hepático, insuficiencia renal, asma, epilepsia, enfermedad psiquiátrica, alcoholismo, diabetes, hipertiroidismo, hipotiroidismo, hemorragia uterina y obesidad)36, 37, 38, 39.
3. Potencial para modificar la función o el número de β2AR o la fisiología uterina (uso de drogas ilícitas, tabaquismo, elevado consumo de cafeína, tratamiento con terapia electroconvulsiva, calcioantagonistas, antiinflamatorios no esteroideos, sulfato de magnesio, glucocorticoides, hormonas tiroideas, betabloqueadores, agonistas beta, dopamina, amiodarona, antidepresivos tricíclicos, inhibidores de la recaptación de serotonina, inhibidores de la monoaminooxidasa, pseudoefedrina, clonidina, alfametildopa). En total se seleccionaron 35 mujeres que presentaron parto pretémino en ausencia de una causa aparente de tal suceso (como resultado hubo el nacimiento de 35 niños prematuros). En el grupo control, se incluyeron 105 mujeres que concluyeron su embarazo entre las 37 y 41 semanas de edad gestacional, sin complicaciones y sin antecedentes de parto pretérmino (como resultado nacieron 105 niños a término). Todas las pacientes firmaron el consentimiento informado y recibieron copia del mismo.
Determinación de los polimorfismos. Para identificar los polimorfismos se obtuvieron 5 ml de sangre venosa periférica con el fin de extraer el ADN de los linfocitos mediante la técnica de Salting Out. Después, con la reacción en cadena de la polimerasa (PCR), se amplificó un segmento del β2AR de 265 pares de bases que incluye cuatro polimorfismos de nucleótido único: dos polimorfismos de la región reguladora del gen (-47 C/T y -20 C/T) y dos de la región codificante (Arg16Gly y Gln27Glu). Se utilizaron como cebadores las secuencias 5´ ctgaatgaggcttccaggcgtc 3´ y 5´ ccagcacattgcca aacacg 3´ (diseño propio). Luego de una desnaturalización inicial del ADN geonómico a 95°C durante 4 minutos, se realizaron 40 ciclos de desnaturalización, alineamiento y extensión a 95°C, 56°C y 72°C, respectivamente, por un minuto para cada uno (termociclador BioRad PTC 100). Los productos de amplificación se sometieron a electroforesis en geles de agarosa al 1.5% y se visualizaron a través de la tinción con bromuro de etidio e iluminación ultravioleta (Figura 1). Cada uno de los polimorfismos se identificó por secuenciación directa con el método de los terminadores de cadena. La PCR para la secuenciación se realizó con los cebadores ya descritos y cada uno de los dideoxinucleotidos que se usaron en la reacción estaba marcado con una sonda fluorescente distinta (3730xl DNA analyzer, Macrogen Inc); (los electroferogramas de dos de los polimorfismos se muestran en la Figura 2).
Análisis estadístico.Se efectuó un estudio de casos y controles no pareado. Se compararon variables como la edad, el peso, la talla y el índice de masa corporal entre el grupo de casos y el grupo de controles. Para cada locus polimórfico, se analizaron las diferentes frecuencias alélicas en tablas de 2 x 2, y a cada una de ellas se le aplicó la prueba exacta de Fisher. Los tres genotipos posibles por cada polimorfismo y los diferentes haplotipos encontrados se analizaron en tablas de 3 x 2, y se hizo la prueba de Chi2. Estas comparaciones se efectuaron con el programa estadístico GraphPad Prism versión 4.00.
Para calcular el desequilibrio de ligamiento, y el principio de Hardy-Weinberg se utilizó el programa estadístico Genepop versión 3.4. Las pruebas estadísticas se establecieron para descubrir, con 34 casos y 102 controles, una diferencia mínima entre grupos de 20%, con un poder estadístico de 80% y una p<0.05.
RESULTADOS
No se encontraron diferencias en cuanto al peso. La media fue 53.82±0.46 kg para los controles y 51.97±0.99 kg para los casos (p=0.0616) (Cuadro 1). Tampoco hubo diferencias significativas en cuanto a la talla entre el grupo de casos y el grupo de controles. Para el primero la media fue 158.5±1.21 cm y para el segundo 159±0.52 cm (p=0.722) (Cuadro 1). La edad fue significativamente menor en el grupo de mujeres con parto pretérmino en comparación con el grupo de mujeres con parto a término (23.06±0.69 años y de 27.13±0.48 años, respectivamente, p<0.0001) (Cuadro 1).
Las frecuencias alélicas y genotípicas para los polimorfismos -47 C/T, -20 C/T, ArgGly y GlnGlu entre los grupos de mujeres con parto a término (casos) y el grupo de mujeres con parto pretérmino (controles) fue la siguiente:
Polimorfismos -47 C/T, y -20 C/T. En el grupo de casos (n=35, alelos=70) se encontraron 55 alelos (78.5%) T y 15 alelos (21.5%) C; en el grupo control 165 alelos (78.5%) T y 45 alelos (21.5%) C (p>0.05) (Cuadro 2). En el grupo de casos se encontró el genotipo T/T en 24 mujeres (68.5%), el genotipo T/C en 8 (23%) y el genotipo C/C en 3 (8.5%); en el grupo control se encontró el genotipo T/T en 64 mujeres (61%), el genotipo T/C en 37 (35%) y el genotipo C/C en 4 (4%) (p>0.05) (Cuadro 3).
Polimorfismo Arg16Gly. En el grupo de casos se encontraron 34 alelos (48.5%) A y 36 alelos (51.5%) G; en el grupo control 90 alelos (43%) A y 120 alelos (57%) G (p>0.05) (Cuadro 2). En el grupo caso se encontró el genotipo A/A en 7 mujeres (20%), el genotipo A/G en 21 (60%) y el genotipo G/G en 7 (20%); en el grupo control se encontró el genotipo A/A en 22 mujeres (21%), el genotipo A/G en 47 (45%) y el genotipo G/G en 36 (34%) (p>0.05) (Cuadro 3).
Polimorfismo Gln27Glu. En el grupo de casos (n=35, alelos=70) se encontraron 55 alelos (78.5%) C y 15 alelos (21.5%) G; en el grupo control 165 alelos (78.5%) C y 45 alelos (21.5%) G (p>0.05) (Cuadro 2). En el grupo de casos se encontró el genotipo C/C en 24 mujeres (68.5%), el genotipo C/G en 8 (23%) y el geno-tipo G/G en 3 (8.5%); en el grupo control se encontró el genotipo C/C en 64 mujeres (61%), el genotipo C/G en 37 (35%) y el genotipo G/G en 4 (4%) (p>0.05) (Cuadro 3).
De las 16 posibles combinaciones entre los diferentes alelos estudiados, sólo se observaron tres haplotipos: TTGC, TTAC y CCGG, tanto para el grupo de casos como para el grupo de controles.
En el grupo de casos (n=35, haplotipos=70), se encontraron 15 haplotipos CCGG (21.4%), 21 haplotipos TTGC (30%) y 34 haplotipos TTCA (48.6%); mientras que en el grupo de pacientes controles (n=105, 210 haplotipos) se encontraron 45 haplotipos CCGG (21.4%), 75 haplotipos TTGC (35.7%) y 90 haplotipos TTCA (42.9%) (p>0.05) (Cuadro 4).
En ninguno de los dos grupos estudiados, se encontraron diferencias significativas entre las frecuencias genotípicas esperadas y observadas, para cada uno de los 4 loci polimórficos (los datos no se muestran). Además, se observó un fuerte desequilibrio de ligamiento entre los diferentes pares de loci polimórficos (Cuadro 5).
DISCUSIÓN
La evidencia derivada de estudios funcionales demuestra la influencia de algunas variantes genéticas de los b2AR sobre los procesos de desensibilización y regulación del número de receptores27, 32, 33. En consecuencia, ha surgido la hipótesis que estos polimorfismos podrían estar asociados con el parto pretérmino, pues estos receptores: (a) tienen un alto nivel de expresión en el músculo liso uterino21, (b) sufren una disminución importante en relación con el trabajo de parto24 y (c) son capaces de mediar la relajación uterina40.
Sin embargo, en el presente estudio no se encontraron diferencias significativas, en las frecuencias alélicas, genotípicas o haplotípicas de estos cuatro polimorfismos de alta prevalencia en la población general del β2AR, entre el grupo de pacientes con parto pretérmino y el grupo de pacientes que terminaron su gestación a término.
Hasta la fecha, sólo se había estudiado la relación de dos polimorfismos de la región codificante del gen de los β2AR con el parto pretérmino. En ninguna de las investigaciones se tuvo en cuenta la posible interrelación de los polimorfismos de la región codificante con los de la región reguladora del gen, desconociendo la importancia que tiene el polimorfismo -47 C/T sobre el número de receptores, mediante la alteración en la regulación de la síntesis de proteínas a un nivel traduccional27.
Este estudio relaciona los polimorfismos -47 C/T y -20C/T e informa haplotipos de cuatro loci polimórficos del β2AR en relación con el parto pretérmino. A pesar de la aplicación de rigurosos criterios de inclusión y de exclusión, y la búsqueda de una población de casos sin ninguna causa identificable de prematuridad (parto pretérmino idiopático), no fue posible evidenciar ninguna asociación entre los polimorfismos de este receptor y el parto pretérmino espontáneo.
Las diferencias en el diseño y metodología, especialmente la laxitud en los criterios de inclusión y exclusión de estudios anteriores, pueden explicar, al menos parcialmente, la diversidad de resultados. Factores como ruptura prematura de membranas ovulares, obesidad, enfermedades sistémicas y uso crónico de medicamentos, son variables de confusión que alteran los hallazgos y trastornan en gran medida la fisiología uterina al influir directa o indirectamente sobre la transcripción de genes de diversas proteínas relacionadas en su función con la actividad contráctil.
En el trabajo de Ozkur et al.18 se observó que el alelo Glu27 representa un factor de riesgo para el parto pretérmino. Esta conclusión se contradice con los hallazgos encontrados in vitro, donde Glu27 protege de la disminución en el número de los receptores que promueven los fármacos β2 agonistas32, 33. Además, los autores no tuvieron en cuenta otros polimorfismos que tienen dominancia sobre este alelo, ni los haplotipos que son más representativos que un solo polimorfismo de nucleótido único29. Los resultados del artículo de Landau et al.17, un estudio relacionado, sugieren que la homocigocidad para Arg16 protege del parto pretérmino. En ese estudio se incluyeron los polimorfismos Arg16Gly y Gln27Glu, y al igual que en el presente trabajo, se apreció el desequilibrio de ligamiento entre Arg16 y Gln27. Sin embargo, en ese estudio se incluyeron fumadoras, con diabetes gestacional, ruptura prematura de membranas ovulares e incluso asmáticas. En ésta última situación comúnmente se emplean fármacos β2 agonistas como broncodilatadores, pero como variables de confusión no se consideró la posibilidad de que estas sustancias pudieran alterar, de acuerdo con la dosis y al tiempo de uso, el comienzo e intensidad de las contracciones uterinas21, 40, el número de los β2AR o su desensibilización41.
Al igual que Landau et al.17, Doh et al.19, encontraron que la homocigocidad para Arg16 protege del parto pretérmino, mientras que el estado homocigoto Glu27 favorece su presentación19. No obstante este estudio sólo tuvo en cuenta como criterios de exclusión la gestación múltiple, la preeclampsia y la etnicidad; incluyó maternas de todas las edades (con un rango hasta los 45 años), con enfermedades crónicas y con ruptura prematura de membranas ovulares. Por tanto, estas conclusiones no son atribuibles exclusivamente a factores genéticos, sino también a muchos otros factores de riesgo ampliamente conocidos, que en este caso representan factores de confusión.
En otro estudio de Landau et al.42, para determinar si los fármacos β2 agonistas eran más efectivos en mujeres con diagnóstico de parto pretérmino y homocigóticas para Arg16, publicado en el año 2005, contrariamente a lo informado por los mismos autores tres años antes17, no se encontraron diferencias en las frecuencias alélicas ni genotípicas para los polimorfismos de las posiciones 46 y 7942.
Este tipo de contradicciones entre los estudios también se ha visto para la relación de las variantes genéticas del β2AR y otras enfermedades complejas como el asma, donde los resultados de los estudios iniciales asociaron diferentes polimorfismos con la enfermedad, y en estudios publicados después se descartó tal asociación. Por ejemplo, D’Amato et al.43 hallaron asociación entre el haplotipo Gly16 y Gln27 y la hiperreactividad bronquial; en cambio otros, como Dewar et al.44 no encontraron ninguna relación entre los polimorfismos de los β2AR y el asma bronquial. En el asma, la enfermedad compleja más ampliamente estudiada en relación con los polimorfismos de los β2AR, en la actualidad se acepta que tales polimorfismos no son un factor de riesgo principal para su presentación clínica. Sin embargo, tales variaciones genéticas probablemente sean importantes en la respuesta terapéutica a los agonistas de los β2AR45, 46. Como la amenaza de parto pretérmino también se maneja con agonistas β2 adrenérgicos, es probable que la respuesta terapéutica a dichos fármacos, con una alta frecuencia de falla para evitar la terminación prematura del embarazo, esté influida por los polimorfismos de los β2AR42.
Al igual que en estudios anteriores, en esta investigación se encontró un fuerte desequilibrio de ligamiento entre los polimorfismos del gen del β2AR. Esto se refleja claramente porque sólo se identificaron tres haplotipos en toda la muestra entre todas las posibles combinaciones entre los diferentes alelos. Sin embargo, el significado biológico de estos hallazgos está por aclarar.
CONCLUSIÓN
Ante la ausencia de una asociación con el parto pretérmino idiopático, estos polimorfismos no parecen participar como predisponentes importantes del parto pretérmino idiopático en estas pacientes. Aunque se necesitarían estudios de mayor envergadura para establecer o descartar definitivamente una relación de baja frecuencia, por el momento la realización de pruebas genéticas de filtro (tamización) para estas variantes en mujeres embarazadas no está justificada.
REFERENCIAS
1. Branum AM, Schoendorf KC. Changing patterns of low birthweight and preterm birth in the United States, 1981-98. Paediatr Perinat Epidemiol. 2002; 16: 8-15.
2. Challis JRG. Mechanism of parturition and preterm labor. Obstet Gynecol Surv. 2000; 55: 650-60.
3. Goldenberg RL. The management of preterm labor. Obstet Gynecol. 2002; 100: 1020-37.
4. Steer, P. The epidemiology of preterm labor-a global perspective. J Perinat Med. 2005; 33: 273-6.
5. Carr-Hill RA, Hall MH. The repetition of spontaneous preterm labour. Br J Obstet Gynaecol. 1985; 92: 921-8.
6. Kristensen J, Langhoff-Roos J, Kristensen FB. Implications of idiopathic preterm delivery for previous and subsequent pregnancies. Obstet Gynecol. 1995; 86: 800-4.
7. Leslie JC, Galvin SL, Diehl SJ, Bennett TA, Buescher PA. Infant mortality, low birth weight, and prematurity among Hispanic, white, and African American women in North Carolina. Am J Obstet Gynecol. 2003; 188: 1238-40.
8. Shiono PH, Klebanoff MA. Ethnic differences in preterm and very preterm delivery. Am J Public Health. 1986; 76: 1317-21.
9. Zhang J, Savitz DA. Preterm birth subtypes among blacks and whites. Epidemiology. 1992; 3: 428-33.
10. Porter TF, Fraser AM, Hunter CY, Ward RH, Varner MW. The risk of preterm birth across generations. Obstet Gynecol. 1997; 90: 63-7.
11. Wang X, Zuckerman B, Coffman GA, Corwin MJ. Familial aggregation of low birth weight among whites and blacks in the United States. N Engl J Med. 1995; 333: 1744-9.
12. Hoffman JD, Ward K. Genetic factors in preterm delivery. Obstet Gynecol Surv. 1999; 54: 203-10.
13. Genc MR, Gerber S, Nesin M, Witkin SS. Polymorphism in the interleukin-1 gene complex and spontaneous preterm delivery. Am J Obstet Gynecol. 2002; 187: 157-63.
14. Simhan HN, Krohn MA, Roberts JM, Zeevi A, Caritis SN. Interleukin-6 promoter -174 polymorphism and spontaneous preterm birth. Am J Obstet Gynecol. 2003; 189: 915-18.
15. Varner MW, Esplin MS. Current understanding of genetic factors in preterm birth. Bjog. 2005; 112 Suppl 1: 28-31.
16. Gibson CS, MacLennan AH, Dekker GA, Goldwater PN, Dambrosia JM, Munroe DJ, et al. Genetic polymorphisms and spontaneous preterm birth. Obstet Gynecol. 2007; 109: 384-91.
17. Landau R, Xie HG, Dishy V, Stein CM, Wood AJ, Emala CW, et al. Beta2-Adrenergic receptor genotype and preterm delivery. Am J Obstet Gynecol. 2002; 187: 1294-8.
18. Ozkur M, Dogulu F, Ozkur A, Gokmen B, Inaloz SS, Aynacioglu AS. Association of the Gln27Glu polymorphism of the β2-adrenergic receptor with preterm labor. Int J Gynaecol Obstet. 2002; 77: 209-15.
19. Doh K, Sziller I, Vardhana S, Kovacs E, Papp Z, Witkin SS. β2-adrenergic receptor gene polymorphisms and pregnancy outcome. J Perinat Med. 2004; 32: 413-7.
20. Liggett SB. β(2)-adrenergic receptor pharmacogenetics. Am J Respir Crit Care Med. 2000; 161 Supl: 197-201.
21. Liu YL, Nwosu UC, Rice PJ. Relaxation of isolated human myometrial muscle by β2-adrenergic receptors but not b1-adrenergic receptors. Am J Obstet Gynecol. 1998; 179: 895-8.
22. Johnson M. Molecular mechanisms of β(2)-adrenergic receptor function, response, and regulation. J Allergy Clin Immunol. 2006; 117: 18-24.
23. Adelwoehrer NE, Mahnert W. Hexoprenaline activates potassium channels of human myometrial myocytes. Arch Gynecol Obstet. 1993; 252: 179-84.
24. Chanrachakul B, Matharoo-Ball B, Turner A, Robinson G, Broughton-Pipkin F, Arulkumaran S, et al. Reduced expression of immunoreactive β2-adrenergic receptor protein in human myometrium with labor. J Clin Endocrinol Metab. 2003; 88: 4997-5001.
25. Méhats C, Tanguy G, Dallot E, Cabrol D, Ferré F, Leroy MJ. Is up-regulation of phosphodiesterase 4 activity by PGE2 involved in the desensitization of b-mimetics in late pregnancy human myometrium? J Clin Endocrinol Metab. 2001; 86: 5358-65.
26. Kobilka BK, Dixon RA, Frielle T, Dohlman HG, Bolanowski MA, Sigal IS, et al. cDNA for the human β2-adrenergic receptor: a protein with multiple membrane-spanning domains and encoded by a gene whose chromosomal location is shared with that of the receptor for platelet-derived growth factor. Proc Natl Acad Sci U S A. 1987; 84: 46-50.
27. McGraw DW, Forbes SL, Kramer LA, Liggett SB. Poly-morphisms of the 5' leader cistron of the human β2-adrenergic receptor regulate receptor expression. J Clin Invest. 1998; 102: 1927-32.
28. Parola AL, Kobilka BK. The peptide product of a 5' leader cistron in the β2 adrenergic receptor mRNA inhibits receptor synthesis. J Biol Chem. 1994; 269: 4497-505.
29. Drysdale CM, McGraw DW, Stack CB, Stephens JC, Judson RS, Nandabalan K, et al. Complex promoter and coding region β2-adrenergic receptor haplotypes alter receptor expression and predict in vivo responsiveness. Proc Natl Acad Sci USA. 2000; 97: 10483-8.
30. Kirstein SL, Insel PA. Autonomic nervous system pharmacogenomics: a progress report. Pharmacol Rev. 2004; 56: 31-52.
31. Liggett SB. Polymorphisms of adrenergic receptors: variations on a theme. Assay Drug Dev Technol. 2003; 1: 317-26.
32. Green SA, Turki J, Bejarano P, Hall IP, Liggett SB. Influence of β2-adrenergic receptor genotypes on signal transduction in human airway smooth muscle cells. Am J Respir Cell Mol Biol. 1995; 13: 25-33.
33. Green SA, Turki J, Innis M, Liggett SB. Amino-terminal polymorphisms of the human β2-adrenergic receptor impart distinct agonist-promoted regulatory properties. Biochemistry. 1994; 33: 9414-9.
34. Dishy V, Sofowora GG, Xie HG, Kim RB, Byrne DW, Stein CM, et al. The effect of common polymorphisms of the β2-adrenergic receptor on agonist-mediated vascular desensitization. N Engl J Med. 2001; 345: 1030-5.
35. Turnes J, Hernández-Guerra M, Abraldes JG, Bellot P, Oliva R, García-Pagán JC, et al. Influence of β-2 adrenergic receptor gene polymorphism on the hemodynamic response to propranolol in patients with cirrhosis. Hepatology 2006; 43: 34-41.
36. Contopoulos-Ioannidis DG, Manoli EN, Ioannidis JP. Meta-analysis of the association of beta2-adrenergic receptor polymorphisms with asthma phenotypes. J Allergy Clin Immunol. 2005; 115: 963-72.
37. Guerra S, Graves PE, Morgan WJ, Sherrill DL, Holberg CJ, Wright AL, et al. Relation of β2-adrenoceptor poly- morphisms at codons 16 and 27 to persistence of asthma symptoms after the onset of puberty. Chest. 2005; 128: 609-17.
38. Jiao H, Dahlman I, Eriksson P, Kere J, Arner P. A common beta2-adrenoceptor gene haplotype protects against obesity in Swedish women. Obes Res. 2005; 13: 1645-50.
39. Wallerstedt SM, Eriksson AL, Ohlsson C, Hedner T. Haplotype association analysis of the polymorphisms Arg16Gly and Gln27Glu of the adrenergic β2 receptor in a Swedish hypertensive population. J Hum Hypertens. 2005; 19: 705-8.
40. King JF, Grant A, Keirse MJ, Chalmers I. β-mimetics in preterm labour: an overview of the randomized controlled trials. Br J Obstet Gynaecol. 1988; 95: 211-22.
41. January B, Seibold A, Whaley B, Hipkin RW, Lin D, Schonbrunn A, et al. β2-adrenergic receptor desensitization, internalization, and phosphorylation in response to full and partial agonists. J Biol Chem. 1997; 272: 23871-9.
42. Landau R, Morales MA, Antonarakis SE, Blouin JL, Smiley RM. Arg16 homozygosity of the β2-adrenergic receptor improves the outcome after β2-agonist tocolysis for preterm labor. Clin Pharmacol Ther. 2005; 78: 656-63.
43. D'Amato M, Vitiani LR, Petrelli G, Ferrigno L, di Pietro A, Trezza R, et al. Association of persistent bronchial hyperresponsiveness with β2-adrenoceptor (ADRB2) haplotypes. A population study. Am J Respir Crit Care Med. 1998; 158: 1968-73.
44. Dewar JC, Wheatley AP, Venn A, Morrison JF, Britton J, Hall IP. β2-adrenoceptor polymorphisms are in linkage disequilibrium, but are not associated with asthma in an adult population. Clin Exp Allergy. 1998; 28: 442-8.
45. Lee DK, Bates CE, Lipworth BJ. Acute systemic effects of inhaled salbutamol in asthmatic subjects expressing common homozygous β2-adrenoceptor haplotypes at positions 16 and 27. Br J Clin Pharmacol. 2004; 57: 100-4.
46. Taylor DR, Kennedy MA. β-adrenergic receptor polymorphisms and drug responses in asthma. Pharmacogenomics. 2002; 3: 173-84.